Выделение азотистых веществ – Обмен азотистых веществ при брожении
Выделение азотистых веществ – Обмен азотистых веществ при брожении
Выделение азотистых веществ – Обмен азотистых веществ при брожении





Обмен веществ (метаболизм) дрожжей
Микроорганизмы осуществляют свои жизненные функции, главным проявлением которых является рост и размножение за счет многочисленных непрерывно происходящих и взаимосвязанных химических реакций, обычно называемых обменом веществ или метаболизмом. Метаболизм представляет собой два типа процессов, а именно:
анаболизм или ассимиляция характеризуется синтетическими реакциями, при которых потребляется энергия, организмы принимают из среды вещества (питание), эти вещества они способны переработать в продукты, компенсирующие потери, вызванные потреблением и расщеплением, и пригодные для образования новых веществ для роста и размножения;
катаболизм или диссимиляция, т. е. сумма реакций разложения, богатых энергией высокомолекулярных веществ, на вещества простейшие, бедные энергией, а освобождающаяся энергия потребляется на процессе ассимиляции.
Метаболизм сахаридов
В обмене веществ дрожжей и всех живых систем вообще большое значение имеют сахара (сахариды), при расщеплении которых получается энергия для физиологических процессов и для биологического синтеза многих веществ. Расщепление сахаров (гликолиз) является одним из основных процессов. Если он протекает при прямом участии кислорода воздуха, т. е. при аэробных условиях, таких, как окислительный обмен веществ, речь идет о процессе, обычно называемом дыханием (respirace). При анаэробных условиях брожение (ферментация) протекает как антиокислительный обмен веществ.
Дыхание и брожение – это ферментативные процессы, сложный механизм которых в начальных стадиях подобен. Они протекают вначале через ряд промежуточных стадий, а затем на определенной стадии разделяются и идут к конечным продуктам своими собственными путями. При дыхании конечным продуктом являются углекислый газ и вода
и при брожении спирт (этанол) и углекислый газ
Количество энергии, освободившейся при этих катаболических (диссимиляционных) процессах, зависит от степени окисления. Чем выше теплота сгорания образующихся продуктов, тем меньше энергии освободилось для клетки. Метаболизм сахаридов (углеводов) и его отношение ко всему обмену веществ выражает следующая схема [5]:
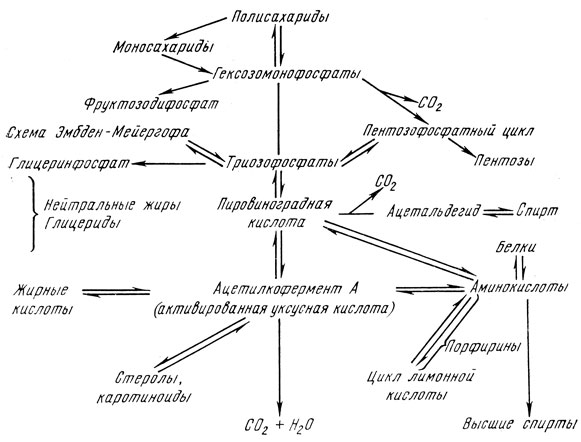
Полисахариды и олигосахариды (мальтоза, сахароза) или сначала расщепляются на моносахариды и фосфорилируются, прямо переходят в фосфаты гексозы. Последний из них фруктозо-1,6-дифосфат расщепляется на два фосфорилированных С3-сахара (по схеме Эмбден-Мейергофа) или уже на предшествующей стадии глюкозо-6-фосфат дегидрогенизируется на 6-фосфоглюконовую кислоту и путем окислительной декарбоксилации перейдет в пентозофосфат, который является голозидным компонентом рибонуклеиновых кислот. Фосфаты пентозы в так называемом пентозофосфатном цикле переходят через гептозы, гексозы, тетрозы в фосфаты триоз и гексоз, через которые присоединяются к схеме Эмбден-Мейергофа.
Из триозофосфата (дигидроксиацетонфосфата) образуется в качестве побочного продукта глицерин, основное вещество для синтеза нейтральных жиров и фосфатидов.
Основной путь расщепления сахаридов ведет от триозофосфата через разные промежуточные стадии к пировиноградной кислоте. При декарбоксилации и восстановлении образуются основные продукты анаэробного гликолиза, т. е. этанол и углекислый газ. Кроме того, пировиноградная кислота, отдает свой углеродный скелет аминокислоте аланина, который образуется в результате трансаминирования.
При аэробных условиях протекает также процесс окисления, в результате которого образуется “активированная уксусная кислота”. При скоплении ацетиловых остатков активированной уксусной кислоты образуются жирные кислоты, стеролы, каротиноиды и одновременно образуется углеродный скелет ряда важных аминокислот. Эти процессы обратимы и поэтому ацетилкофермент А является важным промежуточным веществом расщепления, перестройки и построения сахаридов, белков, жиров, стеролов, каротиноидов и других веществ.
Окончательное превращение ацетиленового остатка в углекислый газ и воду осуществляется в цикле лимонной кислоты, благодаря чему клетка приобретает основную часть энергии. Из промежуточных продуктов α-кетоглютаровой и щавелевоуксусной кислот при аминировании и трансаминировании образуются глютаминовая и аспарагиновая кислоты.
При пивоваренном брожении основным и преобладающим процессом является анаэробный гликолиз (брожение) по схеме Эмбден-Мейергофа-Парнасова, при котором в качестве основных продуктов образуются этанол и углекислый газ. В присутствии кислорода на процесс брожения накладываются аэробные процессы (дыхание), в частности в стадии пировиноградной кислоты цикл лимонной кислоты (Кребса) или в стадии глюкозо-6-фосфата-пентозофосфатный цикл.
При низовом пивоваренном брожении приблизительно 98% сахара сбраживается и 2% используются на процесс дыхания.
Спиртовое брожение (схема Эмбден-Ме йергофа)
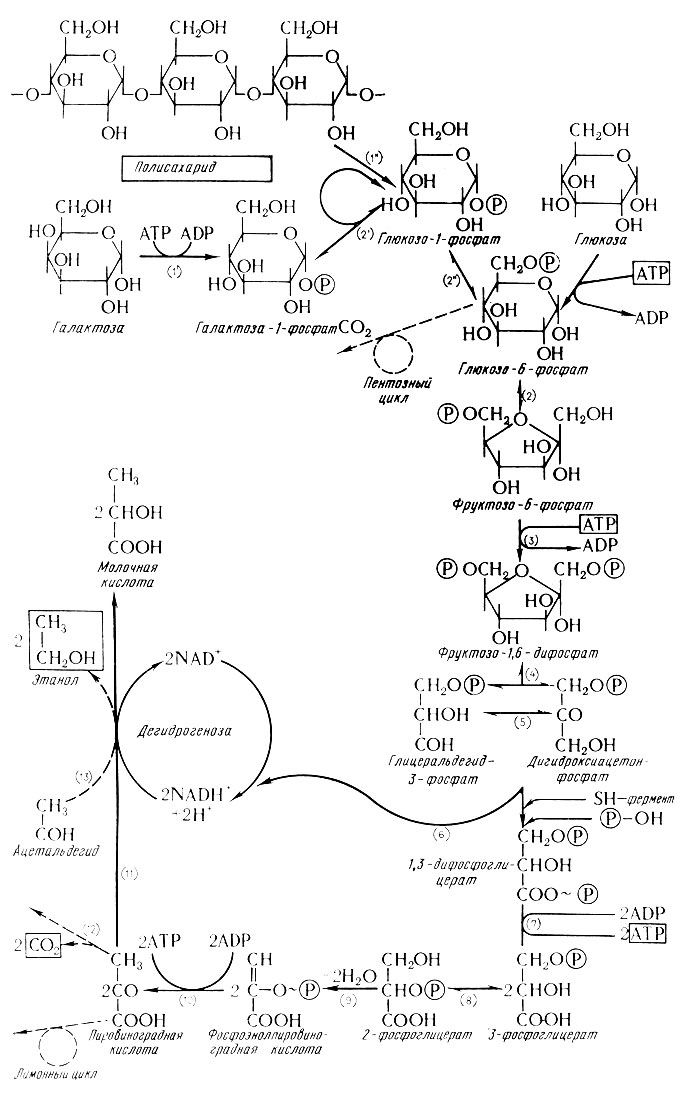
Спиртовое брожение очень сложный процесс, при изучении которого постепенно выяснилось, что он протекает как цепь ре-акций, связанных фосфорилирующим механизмом.
В первой фазе брожения (стадия фосфорилирования) образуются разные фосфаты гексоз. Последний из них (фруктозо-1,6- дифосфат) распадается на два триозофосфата: дигидроксиацетонфосфат и глицеральдегид-3-фосфат. Глицеральдегид-3-фосфат дегидрогенизируется при вмешательстве никотинамидадениндинуклеотида (НАД) и одновременно фосфорилируется в 1,3-фосфорглицериновую кислоту, которая последующей дегидрогенизацией и дефосфорилизацией переходит в пировиноградную кислоту. Кислота в свою очередь декарбоксилируется в углекислый газ и ацетальдегид, который в последней фазе восстанавливается в спирт (этанол). Весь ход спиртового брожения виден по при-веденной по Де Клерку (6) схеме, которая составлена на основе имеющихся данных, относящихся к изучению этого сложного процесса.
Сбраживаемость сахаров различна и зависит от вида сахара и от свойств дрожжей. Сначала считали, что прямо сбраживаются только так называемые зимогексозы, т. е. глюкоза, фруктоза, маноза и условно (после приспособления) также галактоза, при этом все только в оптической D-форме. Олигосахариды считались сбраживаемыми только после расщепления на гексозы соответствующими ферментами. Например, низовые пивоваренные дрожжи содержат инвертазу (сахарозу, β-фруктозидазу-β-D-фруктофуранозид фруктогидролазу, ЕК 3.2.1.26), катализирующую расщепление сахарозы на глюкозу и фруктозу, далее мальтозу (α-глюкозидазу-α-D-глюкозид глюкогидролазу, ЕК 3.2.1.21), которая катализирует расщепление мальтозы на две молекулы глюкозы и, наконец, мелибиазу (α-галактозидазу-α-D-галактозид галактогидролазу, ЕК 3. 2. 1. 23), которая при одновременном присутствии сахарозы расщепляет трисахарид на все три его составляющие, т. е. галактозу, глюкозу и фруктозу. У верховых дрожжей мелибиаза отсутствует и поэтому они расщепляют рафинозу на мелибиозу и фруктозу, так что сбраживают только ее фруктозный компонент ( 1 /3).
В последнее время с помощью хроматографического метода подтвердилось существование трансфераз, способных переносить гексозные единицы с одной молекулы дисахарида или трисахарида на другую, или также внутри молекулы с одной связи на другую. Так, под действием трансглюкозидазы может образоваться например, из сахарозы трисахарид фруктозо-фруктозо-глюкоза или фруктозо-глюкозо-фруктоза. Образовавшиеся таким образом сахара под действием трансфераз расщепляются (сбраживаются) непосредственно ферментами брожения. Сбраживаемость сахаров зависит также от проницаемости клеточной оболочки дрожжей. Известно, что внутрь дрожжей проникают дитрисахариды, а высшие сахара и декстрины никогда.
Согласно суммарному уравнению брожения из 100 г глюкозы теоретически получается 51,1 г спирта (этанола) и 48,9 г углекислого газа. Практически выход всегда ниже и соответствует в среднем 48,6% этанола и 46,4% углекислого газа. Около 2% глюкозы дрожжи ассимилируют и остаток приблизительно 3% переходит в побочные продукты, т. е. ацетилдегид, глицерин, уксусную и молочную кислоту.
Цикл лимонной кислоты
В начале брожения сусло всегда содержит определенное количество растворенного кислорода воздуха, в присутствии которого дрожжи “дышат”. Тем самым изменяется первоначальная схема анаэробного метаболизма. Восстановление ацетилдегида замедляется, так что начинается скапливаться пировиноградная кислота, незначительный излишек которой аэробно декарбонизируется в цикле лимонной кислоты, или в трикарбоксиловом цикле, называемом также по имени его открывателя циклом Кребса.
В реакцию включается следующий комплекс ферментов, катализирующий в присутствии кофермента А образование ацетил- кофермента А из очень небольшого количества пировиноградной кислоты. При его действии на щавелевоуксусную кислоту образуется лимонная кислота, а из нее постепенно кислоты цисаконитовая, L-изолимонная, щавелевоянтарная, α-кетоглутаровая, фумаровая, L-яблочная и, наконец, щавелевоуксусная, которая остается в цикле. Ее реакцией с пировиноградной кислотой начинается новый цикл.
Уже раньше было известно, что при полном исключении дыхания снижается жизнеспособность пивных дрожжей, а тем самым снижаются и их физиологические функции и бродильная активность. Вайнфуртнер [3] приводит, как вывод из новых исследований [15], сведения о том, что энергия, получаемая при дыхании, физиологически неравноценна энергии, полученной при брожении, поскольку без дыхания дрожжи постепенно утрачивают способность к размножению.
Пентозофосфатный цикл
В последнее время обнаружилось, что при дыхании дрожжей до 30% глюкозы расщепляется прямым окислением [16] в следующем так называемом пентозофосфатном или гексозомонофосфатном цикле по схеме Варбурга, Дикенса и Хорекера. При спиртовом брожении он накладывается на схему Эмбден-Майергофа в стадии глюкозо-6-фосфата, который окисляется в 6-фосфоглюконовую кислоту (через δ-лактон). При декарбоксилации через 6-фосфо-3-кетоглутаровую кислоту образуется рибулозо-5- фосфат. Последняя образует с рибозо-5-фосфатом седогептулозо-7-фосфат и глицеральдегид-3-фосфат, который возвращается в нормальную схему Эмбден-Мейергофа. Седогептулозо-7-фосфат расщепляется в эритрозо-4-фосфат и дигидроксиацетон. В присутствии глицеральдегид-3-фосфата образуется фруктозо-6-фосфат, который начинает следующий цикл.
Одним кольцом пентозофосфатного цикла одна молекула глюкозо-6-фосфата декарбонизуется в рибулозо-5-фосфат. При этом восстанавливаются две молекулы трифосфопиридиннуклеотида (ТПН), который снова должен окисляться кислородом воздуха.
Эффект Пастера
Основные изменения в метаболизме дрожжей, связанном с подачей воздуха в процессе брожения (анаэробный и аэробный процесс), первым заметил Пастер. Он обнаружил, что кислород подавляет брожение (образование спирта), однако ускоряет рост (размножение) дрожжей. Это явление известно как эффект Пастера. При аэробных условиях дрожжи не сбраживают (кроме пивных) сахар в этанол, а образуется только углекислый газ; при этом по сравнению с аэробным гликолизом потребление глюкозы намного меньше. По теории Линена [17], диапазон расщепления сахара регулирует концентрация неорганического фосфата и аденозиндифосфата (АДФ).
У пивоваренных культурных дрожжей эффект Пастера не наблюдается [18]. С технологической точки зрения наличие эффекта Пастера свидетельствовало бы о нарушении функций пивоваренных дрожжей.
Метаболизм азотистых веществ
Азотистые вещества в дрожжевых клетках постоянно обновляются. Одновременно с расщеплением протекает синтез белков. В качестве азотистых продуктов питания дрожжевым клеткам служат соли аммония, аминокислоты и низшие пептиды, если они проникают через оболочку клетки.
Для роста, обновления и восстановления живых систем особое значение имеют аминокислоты. Они образуются при введении аминогруппы в α-кетокислоты, которые являются промежуточными продуктами при расщеплении сахаридов. Преимущественную часть потребления аминокислот (около 75%) дрожжи осуществляют прямой ассимиляцией и почти весь остаток дезаминированием по схеме Эрлиха с образованием высших спиртов [19]. Для синтеза белков наиболее важна глютаминовая и аспарагиновая кислоты, аланин и амиды первых двух, т. е. глютамин и аспарагин.
Кроме аминокислот дрожжи ассимилируют также пептиды [20]. Из азота, ассимилированного из сусла дрожжами, около 11 % приходится на пептиды. Поэтому значение пептидов по сравнению с соответствующими аминокислотами меньше, а именно потому, что под действием экзопептидаз они сначала должны расщепляться в простые компоненты.
Внутри дрожжевых клеток аминокислоты подвергаются трансаминированию катализованному трансаминозами, переносящими аминогруппы с одной молекулы на другую. Так, например, аланин образуется путем реакции глютаминовой кислоты с пировиноградной. Высокомолекулярные азотистые вещества образуются конденсацией аминокислот при участии аденозинтрифосфата (АТФ). В пивном сусле аминокислоты являются более важным источником азота, чем аммониевые соединения [21]. Легко ассимилируемыми являются аргинин, лизин, метионин, глютаминовая и аспарагиновая кислоты. И, наоборот, пролин, валин и другие выделяются в среду.
Сусло всегда содержит достаточное количество азотистых веществ. Из 600 мг ассимилированного азота, содержащегося в 1 л сусла (12%-ное), при брожении дрожжи потребляют около 200 мг [22]. В стадии роста содержание азота в дрожжах быстро возрастает, пока не достигнет почти двукратной величины [23] и потом снова постепенно падает вплоть до исходной величины. Дальнейшее уменьшение содержания азота связано с тем, что дрожжи выделяют в среду от 5 до 33% из собственного объема азота, вероятнее всего в виде аминокислот и пептидов.
Метаболизм минеральных веществ
Общее значение минеральных веществ в клеточном организме вытекает из следующих функций:
они поставляют основные (неорганические) элементы для построения органических соединений (углерод, азот, сера и фосфор);
регулируют и поддерживают в организме определенные величины некоторых физических или физико-химических свойств, например прочность клеточной оболочки, осмотическое давление протоплазмы, ионное равновесие, pH, проницаемость клеточной оболочки, растворимость белков, активность ферментов и т. д.;
являются составной частью некоторых биологических катализаторов, главным образом ферментов (железо, медь), витаминов (кобальт), красителей (магний), активируют или ингибируют многие ферментативные реакции (магний, железо, медь, кальций, калий, натрий, кобальт, цинк и т. д.) и тем самым прямо вмешиваются в метаболические процессы.
Выделение конечных продуктов азотистого обмена
Мочевая кислота является одним из наиболее важных конечных продуктов азотистого обмена у человека. В норме ее концентрация в сыворотке крови у мужчин составляет 0,27— 0,48 ммоль*л1, у женщин 0,18—0,38 ммоль*л-1; суточная экскреция с мочой колеблется от 2,3 до 4,5 ммоль (400—750 мг). У человека экскретируется мочевая кислота, у многих млекопитающих имеется фермент уриказа, которая окисляет мочевую кислоту до аллантоина. В теле здорового человека в сутки образование и выделение мочевой кислоты составляет от 500 до 700 мг. Большая часть мочевой кислоты (до 80 %) образуется в результате метаболизма эндогенных нуклеиновых кислот, лишь около 20 % связано с пуринами, поступающими с пищей. Почки за сутки экскретируют около 500 мг мочевой кислоты, 200 мг удаляются через желудочно-кишечный тракт.
Мочевая кислота свободно фильтруется в клубочках почки у человека; в почечных канальцах она подвергается как реабсорбции, так и секреции. В нормальных условиях до 98 % профильтровавшейся мочевой кислоты реабсорбируется.
Изучены механизмы канальцевого транспорта мочевой кислоты и способы регуляции этого процесса. При реабсорбции эта кислота переносится через мембрану щеточной каемки и базолатеральную мембрану клетки проксимального канальца. He исключена возможность всасывания части мочевой кислоты через зону клеточных контактов. Секреция уратов из крови в просвет проксимального канальца зависит от наличия в базальной плазматической мембране анионообменного механизма, обеспечивающего поступление мочевой кислоты в клетку и ее последующее выведение через мембрану щеточной каемки в просвет канальца.
Увеличение клиренса и экскреции мочевой кислоты наблюдается при увеличении диуреза, вызванном введением воды, маннитола, физиологического раствора. Одной из причин урикозурии является увеличение объема внеклеточной жидкости и снижение проксимальной реабсорбции; уменьшение экскреции мочевой кислоты описано при усилении реабсорбции натрия в проксимальном канальце, например при застойной сердечной недостаточности. Введение малых доз салицилатов и фенилбутазона сопровождается снижением экскреции уратов почкой и развитием гиперурикемии, в больших дозах оба эти вещества вызывают урикозурию. Объяснить этот парадоксальный эффект можно тем, что система секреции высокочувствительна к действию этих веществ и они блокируют ее уже в малых дозах, выделение уратов снижается; при введении больших количеств препаратов ингибируется система реабсорбции мочевой кислоты и наблюдается урикозурический эффект. Реабсорбция и секреция мочевой кислоты угнетаются пробенецидом, секреция — пиразиноевой кислотой.
Мочевая кислота имеет рКa 5,75, т.е. при pH мочи ниже этой величины ее растворимость очень мала, она становится недиссоциированной. Так как pH мочи в ее конечных отделах может снижаться до величин, равных 4,4, то это будет способствовать образованию малорастворимых форм мочевой кислоты. Образованию ее кристаллов благоприятствует также всасывание больших количеств воды в почечных канальцах и гиперурикемия, способствующая увеличению концентрации мочевой кислоты в моче. Однако в почечных канальцах у здоровых людей создаются условия, при которых не происходит образования почечных камней. Механизм этого явления неясен.
Циркадный ритм экскреции мочевой кислоты напоминает ритм выделения натрия — в ночные часы выведение мочевой кислоты почти в 2 раза меньше, чем утром в период с 1 до 10 ч.
При анализе причин повышенной концентрации мочевой кислоты в крови (гиперурикемия) необходимо проанализировать следующие возможности: 1) увеличение скорости синтеза мочевой кислоты, 2) уменьшение клубочковой фильтрации, 3) увеличение канальцевой реабсорбции, 4) снижение канальцевой секреции. Следует учитывать, что некоторые фармакологические средства могут влиять на транспорт мочевой кислоты в почечных канальцах. Так, пиразинамид быстро уменьшает экскрецию мочевой кислоты и вызывает гиперурикемию.
Креатинин. В сыворотке крови у здоровых мужчин концентрация креатинина составляет 0,6-1,2 мг*100 мл-1 (0,053—0,106 ммоль*л-1), у женщин — 0,5-1,1 мг*100 мл-1 (0,044—0,097 ммоль*л-1). Суточная экскреция креатинина почками у мужчины (70 кг) составляет 0,98—1,82 г (8,7—16,1 ммоль), у женщин на 20—25 % меньше. Креатинин образуется из креатинфосфата, являющегося важнейшим компонентом мышечных клеток. После отщепления фосфата от креатинфосфорной кислоты образуется креатин, потеря молекулы воды приводит к появлению креатинина.
Количество креатинина, ежедневно образующегося в организме человека, является довольно постоянной величиной, которая зависит от мышечной массы тела. Поэтому содержание креатинина в крови и его выделение почками определяются полом, возрастом, развитием мышечной массы, интенсивностью обмена. В меньшей степени оно зависит от рациона, определенную роль играет содержание мяса в пище.
Креатинин полностью фильтруется в почечных клубочках. Небольшие его количества сек-ретируются клетками проксимального канальца, в некоторых случаях эта величина достигает 28 % по отношению к количеству креатинина, поступившего в просвет нефрона при фильтрации. В эксперименте показано, что секреция креатинина угнетается при введении гиппурана, диодраста, пробенецида. Система секреции креатинина подчинена гормональному контролю. При введении человеку кортизона клиренс креатинина снижается до величины одновременно измеренного клиренса инулина, что свидетельствует об угнетении секреции креатинина. При низкой скорости мочеотделения (меньше 0,5 мл*мин-1) значительные количества креатинина могут реабсорбироваться.
Однако следует признать, что в обычной клинической практике измерение клиренса эндогенного креатинина служит довольно точным отражением величины клубочковой фильтрации. Суточное образование креатинина в организме меняется мало, поэтому при поражении клубочков уменьшается объем фильтруемой жидкости и нарастает концентрация креатинина в плазме крови. В клинической практике изменение концентрации креатинина в крови позволяет судить о состоянии процесса гломерулярной фильтрации в почке.
Мочевина является у человека важнейшим конечным продуктом азотистого метаболизма. В обычных условиях потребление белка в сутки составляет около 100 г, в нем содержится до 16 г азота. Почти 90 % азота выделяется с мочой в виде мочевины, что составляет 0,43—0,71 моль мочевины в сутки.
Экскретируемая мочевина необходима для процесса осмотического концентрирования мочи. В почечных клубочках мочевина свободно фильтруется и поступает в просвет канальца в той же концентрации, что и в воде плазмы крови (15—38,5 мг*100 мл-1, или 2,5-6,4 ммоль*л-1). Стенка проксимального сегмента нефрона проницаема для мочевины, и к концу этого отдела реабсорбируется около половины профильтровавшейся мочевины. К началу дистального извитого канальца в жидкости просвета нефрона количество мочевины превышает поступившее с ультрафильтратом. Это означает, что в каких-то участках петли Генле из околоканальцевой жидкости она через стенку нефрона вновь поступает в его просвет. Специальными исследованиями было показано, что это не обусловлено активной секрецией мочевины, а зависит от ее движения по концентрационному градиенту из межклеточного вещества, где высоко содержание мочевины, в канальцевую жидкость с меньшей ее концентрацией. Стенка дистального канальца и начальных отделов собирательных трубок слабопроницаема для мочевины. Собирательные трубки мозгового вещества почки при водном диурезе реабсорбируют мало мочевины, но в присутствии вазопрессина проницаемость их стенки для мочевины резко возрастает, она всасывается в мозговое вещество почки, а ее экскреция уменьшается. Эти данные позволяют адекватно объяснить известный в клинике факт, что очищение от мочевины при диурезе меньше 2 мл*мин-1 низкое, но быстро возрастает и приобретает стандартное значение, если во время водного диуреза (т.е. при малой концентрации или отсутствии в крови вазопрессина) мочеотделение становится выше 2—3 мл*мин-1.
Данные об увеличении проницаемости собирательных трубок мозгового вещества почки для мочевины при воздействии вазопрессина дают возможность понять причину увеличения содержания мочевины в дистальном канальце и само явление рециркуляции мочевины. В собирательных трубках коры почки всасывание воды через канальцевую стенку, непроницаемую для мочевины, приводит к повышению ее концентрации в канальцевой жидкости. Когда под влиянием вазопрессина возрастает проницаемость стенки собирательной трубки для мочевины, она начинает всасываться по концентрационному градиенту в мозговое вещество, где увеличивается ее содержание. Из внеклеточной жидкости мочевина проникает в просвет тонкого нисходящего отдела петли Генле и, возможно, тонкого восходящего отдела петли Генле юкстамедуллярных нефронов, что приводит к появлению в дистальных канальцах больших количеств мочевины. Благодаря этому функционирует система кругооборота, рециркуляции мочевины, которая в значительной степени определяет степень осмотического концентрирования мочи и уровень экскреции мочевины почкой.
Метаболизм азотистых веществ
Для размножения дрожжей и необходимого для этого строительства нового клеточного вещества дрожжам требуется азот. В начальной фазе брожения низкомолекулярные пептиды гидролизуются и утилизируются дрожжами. Во время основной стадии брожения главный, но не единственный источник азота составляют аминокислоты. Дипептиды перерабатываются медленнее, чем аминокислоты. В конце брожения даже при наличии аминокислот вновь начинается ассимиляция пептидов. Аминокислоты важны не только для биосинтеза протеинов дрожжей, но и для образования пермеаз и других ферментов. В сусле для создания необходимых условий для размножения дрожжей и протекания брожения в нужном направлении должно содержаться достаточное количество аминокислот и пептидов.
3.2.2.1. Усвоение аминокислот дрожжами происходит с помощью пермеаз в определенной последовательности. Через некоторое время, за которое дрожжи потребляют половину количества каждой аминокислоты, их можно разделить на четыре группы:
· группа А: глютаминовая и аспараги-новая кислоты, аспарагин, глютамин, се-рин, треонин, лизин, аргинин;
· группа Б: валин, метионин, лейцин, изолейцин, гистидин;
· группа В: глицин, фенилаланин, тирозин, триптофан, аланин, аммиак;
· группа Г: пролин.
Если первые три группы абсорбируются довольно быстро, то пролин дрожжи практически не усваивают. Деление на эти группы действует для дрожжей верхового брожения; для дрожжей низового брожения хотя и имеет место аналогичное распределение аминокислот по группам, в исследованных дрожжах выявлено более позднее усвоение валила и гистидина и наблюдается нестабильное поведение аргинина.
На последовательность усвоения аминокислот оказывают влияние системы пермеаз. Первоначально усвоенная универсальная аминокислота пермеаза (УАП) во время первой стадии брожения еще не синтезируется, так как в сусле еще присутствуют ионы аммония. Аминокислоты группы А и, вероятно, группы Б характеризуются более специфичными транспортными системами, чем УАП. После усвоения ионов аммония из сусла образуется УАП, и все аминокислоты за исключением одной аминокислоты группы Г (пролина) усваиваются по этой транспортной системе дрожжевой клеткой. Выяснилось, однако, что на эффективность абсорбции аминокислот пермеазами влияет состав жирных кислот фосфолипидов в мембране цитоплазмы дрожжевой клетки. Этот состав жирных кислот в ходе брожения изменяется, причем отсутствие кислорода способствует строительству клеточных мембран со все увеличивающейся долей остатков насыщенных жирных кислот, которые при наличии ненасыщенных жирных кислот сусла также потребляются для строительства клеточных стенок. При их дефиците эффективная аэрация может даже вызвать синтез ненасыщенных кислот из насыщенных.
Процесс усвоения аминокислот во время брожения таким образом проходит многопланово, однако при брожении потребление аминного азота зависит не столько от содержания какой-либо отдельной аминокислоты, а скорее от общего содержания ассимилируемого азота.
3.2.2.2. Вместе с тем значение отдельных аминокислот важно и само по себе. Аминокислоты в значительном объеме ассимилируются в ненарушенном состоянии, однако в результате трансаминировання дрожжами они преобразуются в такие аминокислоты, которые именно в этот момент времени наиболее необходимы для строительства клеточного белка. Для этого служат не только углеродные каркасы аминокислот, но и каркасы простых Сахаров, оксикислоты которых при окислительном метаболизме углеводов образуются как промежуточные продукты реакции (например, α-кетоглутаровая кислота в фазе 15 дает глютаминовую кислоту, щавелево-уксусная кислота – аспарагиновую, а пировиноградная кислота – аланин). В связи с этим одни аминокислоты, α-кетокислоты которых важны для синтеза аминокислот, должны присутствовать в достаточном количестве, тогда как другие, несмотря на их вклад в содержание общего ассимилируемого азота, не столь важны. Лизин, гистидин, агринин и лейцин продуцируют оксикислоты, которые могут ассимилироваться только определенными аминокислотами субстрата. Нехватка этих аминокислот может изменить белковый обмен дрожжей и отрицательно повлиять на качество пива. Концентрация изолейцина, валина, фенилаланина, глицина, аланина и тирозина в сусле важна из-за того, что на более поздних стадиях брожения подавляется синтез Сахаров из акетокислот.
При этом они должны извлекаться из углеродного каркаса соответствующих аминокислот. С другой стороны, слишком низкое их содержание может отрицательно влиять на качество пива. Третья группа аминокислот для метаболизма дрожжей имеет небольшое значение: аспарагиновая к и с л о т а , глютаминовая кислота, аспарагинн, глютамин, треонин, серии и метионин на первых стадиях брожения извлекаются преимущественно из углеродных каркасов аминокислот, а на последней стадии – из кетокислот Сахаров.
К этой группе можно отнести и пролин, так как его концентрация большого значения не имеет.
Дефицит указанных групп аминокислот проявляется в усиленном использовании α-кетокислот углеводного метаболизма. Оксикислоты, высвобождающиеся при этом путем дезаминирования аминокислот, декарбоксилируют в альдегид, который имеет на один атом углерода меньше, чем первоначальная кетокислота, и затем восстанавливаются до спирта (механизм Эрлиха). Это приводит к увеличению содержания высших спиртов и тем самым оказывает влияние на качество пива (см. раздел 7.4.2.2). Избыток аминокислот также вызывает усиленное образование побочных продуктов (см. раздел 3.2.6).
3.2.2.3. Метаболизм азотистых веществ при брожении. В 12 %-ном сусле, приготовленном только из солода, содержится около 1000 мг азота/л. Несоложеное сырье (рис и кукуруза) вызывает снижение содержания азота, причем около 60 % приходится на долю низкомолекулярного азота; α-аминный азот составляет 20-23 %, то есть в сусле из соложеного зерна – 200-260 мг/л.
Снижение содержания азота при нормальном брожении составляет 250-320 мг/л, и таким образом в пиве, как правило, остается еще от 680 до 750 мг/л азота. Основное снижение содержания азота происходит вследствие его усвоения дрожжами, включающего не только α-аминный азот, но и низкомолекулярные пептиды. Содержание осаминного азота уменьшается на 100-120 мг/л. Из-за снижения значения pH в ходе брожения 50-70 мг высокомолекулярных азотистых веществ/л выпадают в осадок, адсорбируются на поверхности дрожжей или захватываются пузырьками углекислого газа и переходят шапку пены (деку). Дрожжи, однако, не только потребляют азотистые вещества, но и вновь выделяют часть из них в виде аминокислот и пептидов. С учетом этого количества азота дрожжи перерабатывают около 40 % азота сусла.
Метаболизм жиров
Липиды дрожжей вместе с белком образуют клеточные мембраны дрожжей. При этом речь идет о фосфолипи-дах, стеринах (эргостерине, цимостерине), гликолипидах и др. Липиды составляют около 80 % CB клеточных стенок. Так как масса дрожжей во время брожения увеличивается в 4 – 6 раз, то наряду с белком должны быть синтезированы и липиды, для чего требуется молекулярный кислород.
3.2.3.1. Образование жирных кислот начинается с активирования уксусной кислоты, образующейся при окислительном декарбоксилировании пирувата. Путем конденсации ацетилкоА и нескольких молекул малонилкоА в процессе синтеза жирных кислот образуются насыщенные жирные кислоты. Ненасыщенные жирные кислоты образуются путем дегидрирования насыщенных жирных кислот с одинаковой длиной цепочек при участии НАДФ H2 и молекулярного кислорода. При этом возможно формирование только одной двойной связи (между 8-м и 9-м атомами углерода). На синтез жирных кислот положительно влияют фосфаты, магний, биотип и пантотеновая кислота.
3.2.3.2. Значение жирных кислот в метаболизме дрожжей. Высокомолекулярные ненасыщенные жирные кислоты, присутствующие в клеточной стенке в виде липидов, в частности стерин (например, эргостерин), способствуют усвоению питательных веществ в растворенной или диспергированной форме. При недостатке таких липидов поглощение аминного азота становится невозможным, даже если в сусле содержится достаточное количество аминокислот. Транспортировка фосфата через клеточную мембрану также зависит от содержания в ней липидов. Кроме того, ненасыщенными жирными кислотами активируются важные для реакций фосфорилирования АТФ-ферменты. Таким образом, липиды в той или иной степени важны для основного пути расщепления глюкозы по схеме Эмбдена-Мейергофа-Парнаса.
Существенное влияние жирных кислот на процессы, происходящие во время брожения, свидетельствует о том, что в клетке должно присутствовать некоторое минимальное число ненасыщенных высокомолекулярных жирных кислот. Они могут быть внесены с суслом, что, однако, в последующем вызывает проблемы со стабильностью вкуса пива. Стимулировать синтез этих жирных кислот необходимо за счет хорошего снабжения кислородом в начале брожения.
В сусле также присутствуют насыщенные и ненасыщенные среднемолекулярные жирные кислоты (C6-C12). Они также участвуют в процессе метаболизма дрожжей, причем С2-фрагмеиты используются через ацетил-коА и малонил-коА для синтеза высокомолекулярных жирных кислот.
3.23.3. Жирные кислоты и образование сложных эфиров. Образование сложных эфиров в ходе брожения (см. раздел 3.2.6.2) может подавляться повышенным содержанием ненасыщенных жирных кислот в сусле. С их помощью образуется больше клеточной массы дрожжей, что обусловливает утилизацию богатых энергией соединений в виде кофермента А, которого затем не хватает для образования сложних эфиров. В некоторых условиях, однако, насыщенные кислоты могут оказывать обратное действие – например, стеариновая и пальмитиновая кислоты в форме коА-комплексов способны выступать в качестве ингибитора синтеза жирных кислот. Ненасыщенные жирные кислоты снижают также образование среднемолекулярных жирных кислот (по-видимому, этот механизм сходен с вышеописанным).
3.2.3.4. Синтез глицерина основан на расщеплении углеводов (схема Эмб-дена-Мейергофа-Парнаса, фаза 4). Образующийся при этом диоксиацетонфосфат восстанавливается с помощью НАДН в глицеринфосфат и фосфоэстеразой переводится в глицерин. Глицерин, образующийся при расщеплении жиров, наоборот, вводится в анаэробный углеводный обмен. Свободные жирные кислоты окисляются до CO2 и воды, однако степень этой реакции зависит от степени расщепления углеводов.
Источники:
http://wine.historic.ru/books/item/f00/s00/z0000029/st086.shtml
http://sunmuseum.ru/nefrologiya/3172-vydelenie-konechnyh-produktov-azotistogo-obmena.html
http://lektsii.org/4-8252.html





