Влияние аэрации – Условия развития и активности молочных бактерий вина
Влияние аэрации – Условия развития и активности молочных бактерий вина
Условия развития и активности молочных бактерий вина
Содержание материала
СПОСОБЫ ИССЛЕДОВАНИЯ РОСТА БАКТЕРИЙ
Бактериальная популяция определяется двумя параметрами: микробиальной плотностью, т. е. массой клеток на единицу объема, и клеточной концентрацией, т. е. числом клеток на единицу объема. Возрастание этих двух параметров отражает рост бактерий. Масса клеток выражает массу синтезированного органического вещества, концентрация — число клеточных делений. В гл. 7 было показано на примере дрожжей, что для роста микроорганизмов необходимо сочетание определенного числа факторов и условий.
Понятие «ограничивающий фактор» было определено в гл. 7, как любой фактор, отсутствие или недостаток которого влекут за собой остановку роста. Определены также различные фазы роста: скрытое состояние, ускоренное развитие, экспоненциальная или логарифмическая фаза, замедление, устойчивая фаза и отмирание (см. рис. 7.1).
Подсчет общего количества клеток и числа живых клеток
Для исследования размножения и активности молочнокислых бактерий можно использовать способы, аналогичные тем, какие применяют в отношении дрожжей. Метод прямого подсчета клеток с помощью гематиметра Маласеза может также применяться к бактериям, используя увеличение в 600 раз; подсчет стрептококков или стрептобацилл остается приблизительным, так как невозможно подсчитать элементы цепочек; в зависимости от их длины результаты могут иметь большие расхождения. Кроме того, можно определять число бактерий по отношению к дрожжам, которые легче поддаются подсчету, например, в молодом вине.
Камера счетчика клеток Салумбини разделена на 400 маленьких квадрат- ных чашечек глубиной 0,04 мм и площадью 0,0025 мм2, т. е. объемом 1/10 000 мм 3 каждая. Бактериальная суспензия фиксируется на формальдегиде и окрашивается метиленовой синью; через 5 мин покоя суспензию рассматривают под микроскопом. Трудности представляют наводка на фокус и определение местонахождения бактерий., Наряду с другими исследованиями авторы отказались от метода прямого подсчета и предпочли способ, основанный на нефелометрических измерениях с эталонированием по массе.
Известно отношение между мутностью бактериальных суспензий и сухой массой бактерий; однако форма, в зависимости от того, кокки это или бациллы, и величина клеток могут исказить истинную картину. При очень тщательной работе в одних и тех же условиях среды, окраски и т. д. помутнение, измеренное нефелометром, можно выразить в сухой массе бактерий, находящихся в состоянии суспензии, в соответствии с заранее построенным графиком (Меламед, 1962). Для удобства работы можно использовать одну и ту же кривую для всех бактерий, хотя и существуют расхождения (в среднем около 10%) между бактериями различной формы. На рис. 12.1 представлена кривая среднего типа. В табл. 12.1 приведены отношения между массой бактерий и числом клеток для двух молочнокислых бацилл; в табл. 12.2 показано влияние формы и величины бактерий на определение методом нефелометрии. 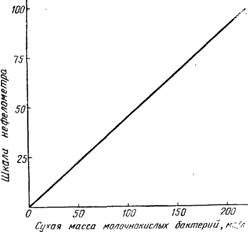
Рис. 12.1. Калибровочная кривая зависимости между сухой массой бактерий молочнокислого брожения в суспензии и оптической плотностью, определенной прямым отсчетом на шкале нефелометра.
Число живых бактерий определяют путем подсчета на чашках Петри. Этот способ труднее реализовать, и он менее точен, чем при работе с дрожжами. Он позволяет приближенно вычислять «жизнеспособность» культур, но не может быть мерой их реального роста. Размножаются не все живые клетки, а некоторые колонии могут возникнуть из групп клеток. Такой метод, который позволил, например, следить за поведением молочнокислых бактерий, введенных в вино, дает лишь сравнительные результаты. Когда живые бактерии находятся в большом объеме жидкости (например, в осветленных винах), предпочтительно использовать фильтрующие мембраны; нужно, чтобы состав питательной среды, на которую помещают мембрану, подходил для развития молочнокислых бактерий вина; работу проводят в атмосфере углекислого газа (Пейно и Сапис-Домерк, 1972).
Эволюция молочнокислых брожений
За развитием культуры можно также следить путем периодического определения одного из поглощаемых или образуемых элементов. В случае молочнокислого сбраживания сахаров определяют молочную кислоту или, что проще, увеличение общей кислотности. При яблочно-молочном брожении вина можно проследить исчезновение яблочной кислоты, применяя хроматографию или количественный микробиологический, или энзиматический анализ; можно, наконец, определять количество углекислого газа манометрическим методом или применением специального электрода (Лонво, 1975).
Отношение между мутностью бактериальной суспензии и формой и величиной клеток
Приблизительные размеры, мкм
Масса бактерий (в мг/л), вызывающих одно и ТО же значение помутнения (75 делений нефелометра)
Таблица 12.1
Отношение между массой молочнокислых бактерий Lactobacillus hilgardii и числом клеток
Число клеток на 1 см*
Влажная масса,* мг/л
Число клеток на 1 мг влажной массы
Сухая масса, мг/л
Число клеток на 1 мг сухой массы
Штамм ВС 2 Штамм ВZ 14
Масса остатка от центрифугирования, после обезвоживания.
Таблица 12.2
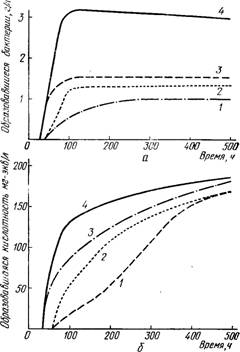
Рис. 12.2. Эволюция роста бактерий, определенная:
а — по сухой массе бактерий, образовавшихся во время молочнокислого сбраживания сахаров; б — по увеличению кислотности во время молочнокислого сбраживания сахаров: 1 — Реdiococcus cerevisiae; 2 — Leuconostoc oinos A+; 3 — Lactobacillus casei; 4 — Lactobacillus hilgardii.
При изучении молочнокислого брожения полной содержащей сахар питательной среды (разбавленное виноградное сусло, обогащенное 5 г/л дрожжевого экстракта и доведенного до рН 4,4), засеянной бактериями, выделенными из вина, в количестве от 30 000 до 50 000 на 1 см 3 при температуре 25° С (рис. 12.2), можно сделать следующие замечания:
а) помутнение, которое можно измерить, проявляется через 24—48 ч после засева; при прочих равных условиях скрытая фаза более продолжительна у кокков; гетеро- или гомоферментативный характер бактерий не оказывает на этот фактор никакого влияния;
б) максимальной численности популяция достигает у молочнокислых бацилл через 4 дня, у кокков за 8— 12 дней; 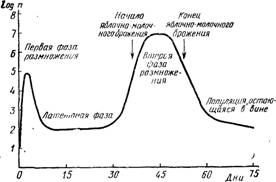
Рис. 12.3. Схема эволюции роста бактерий и яблочно-молочиого брожения при виноделии по красному.
в) урожаи бактерий выше у гетероферментативных видов; массовые значения образующихся гетероферментативных бацилл в 2 раза больше, чем у гомоферментативных бацилл;
г) образование кислотности начинается не сразу; жидкость непрозрачна, в то время как еще не образовалась .концентрация кислотности, достаточная для количественного определения;
д) образование кислотности происходит интенсивно после того, как популяция. достигнет стационарной фазы; кислотность может удвоиться, начиная с момента, когда констатируют максимальный рост бактерий. По истечении 20 дней подкисление все еще продолжается. Не отмечается параллелизма, который существует, например, между спиртовым брожением и размножением дрожжей. Бактерии растут быстрее, чем дрожжи, но имеется расхождение, разрыв между образованием молочной кислоты и ростом;
е) максимальные значения образующейся кислотности у различных бактерий мало различаются .между собой, во всяком случае, они менее изменчивы, чем максимальные значения массы бактерий.
Когда анализируют процесс спонтанного роста бактерий с момента начала переработки винограда посредством указанных выше количественных способов, обычно различают два последовательных цикла роста, которые схематически отражены на рис. 12.3. Первый начинается в первые часы брожения на мезге и протекает параллельно с развитием дрожжей; размножение бактерий прекращается с образованием спирта, и популяция бактерий претерпевает очень сильное уменьшение. Число живых клеток, остающихся в новом вине после спиртового брожения, может сильно колебаться. Веч (1973) сообщает, что у швейцарских вин это число колеблется от 100 до 80 000 на 1 см 3 ; 2/3 вин имеют свыше 10000 живых бактерий на 1 см 3 . Следующий за этим латентный период является более или менее длительным. В отдельных редких случаях могут быть совмещения по времени спиртового и яблочно-молочного -брожения, что нежелательно; чаще всего латентный период длится несколько дней или несколько недель, если при этом выступает какой-либо ограничивающий фактор (сернистый -ангидрид, неблагоприятная темпера- тура); скрытый период может продолжаться в течение нескольких месяцев.
После этой фазы размножение возобновляется и вызывает сбраживание яблочной кислоты. На первой стадии образование молочной кислоты идет слабо. Яблочно-молочное брожение проявляется некоторой задержкой размножения клеток. Разложение яблочной кислоты начинается только тогда, когда рост достигает логарифмической фазы; оно продолжается во время стационарной фазы и даже в фазе замедления. Когда популяция слаба, яблочная кислота не расходуется. Похоже, что численность популяции должна превзойти 1 млн. клеток на 1 см 3 , чтобы яблочно-молочное брожение действительно началось. Фактически речь идет не о настоящем брожении, поскольку оно не является источником энергии.
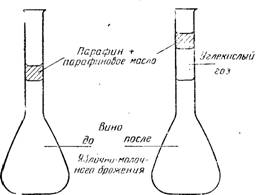
Рис. 12.4. Приспособление, позволяющее экспериментально обнаружить начало яблочно-молочного брожения благодаря образующемуся пузырьку углекислого газа.
Затем после исчезновения яблочной кислоты популяция уменьшается более или менее быстро, и наконец в вине остается популяция живых клеток, численность которой зависит от их рН, степени сульфитации, способов осветления (Мартиньер и сотрудники, 1974).
Чтобы проследить эволюцию яблочно-молочного брожения, в лабораторных условиях было использовано следующее приспособление. Засеянную питательную среду или вина, подлежащие исследованию, помещали в колбы вместимостью 100 или 200 см 3 с длинной тонкой калиброванной шейкой. Их наполняют до калибровочной метки и закрывают толстым слоем смеси, состоящей на 2/3 из парафина и на 1/3 из парафинового масла, которую сжижают легким нагреванием. Затем колбы ставят в термостат при 25° С. При этой температуре смесь затвердевает и сохраняет консистенцию пасты. Такое приспособление позволяет наблюдать пузырек углекислого газа, образующийся под парафиновой пробкой, и фиксировать его объемы, которые заставляют пробку подниматься вверх по горловине колбы (рис. 12.4). Исследуемые среды предварительно очищают от углекислого газа путем взбалтывания под вакуумом. Затем во избежание вмешательства дрожжей в вино вводят актидион из расчета от 2 до 5 мг/л. Система обтюрации действует надежно только при температуре 25° С.
Этот способ особенно чувствителен для определения момента начала яблочно-молочного брожения и позволяет быстро делать большое число сравнений. Этот способ применим и тогда, когда хотят оценить шансы еще кислого вина подвергнуться спонтанному яблочно-молочному брожению; для этого образец шина, помещенный в такую колбу, ставят в термостат и следят за появлением первого пузырька под парафином. Следует подтвердить аналитически исчезновение яблочной кислоты и титруемой кислотности, так как образование углекислого газа даже без участия дрожжей, нельзя рассматривать как явление специфическое для яблочно-молочного брожения.
Чтобы точнее проследить этот феномен, можно использовать углекислотный электрод, который позволяет количественно определять углекислый газ, растворенный в жидкости (Лонво и Риберо-Гайон, 1973); углекислый газ диффундирует через тефлоновую мембрану в электролит, вызывая изменение рН, которое регистрируется. Эти авторы воспользовались аппаратом, созданным для количественного анализа углекислого газа в крови; результаты, выраженные в величинах парциального давления, могут быть представлены в виде концентрации на 1 л.
Влияние аэрации и перемешивания на рост и развитие аэробных термофильных бактерий
Одним из важнейших факторов, определяющих рост и развитие термофильных микроорганизмов, является скорость поступления кислорода и его концентрация в культуральной среде. Степень ограничения роста аэробных организмов при недостатке кислорода зависит от температуры выращивания. Растворимость кислорода в воде увеличивается с понижением температуры, поэтому рост микроорганизмов при более низких температурах не ограничивается содержанием кислорода в такой степени, как в случае инкубации при высоких температурах. Этим и объясняется тот факт, что общий урожай организмов, выращенных при низких температурах, часто оказывается выше, чем урожай микроорганизмов, выращенных при более высоких температурах, хотя скорость роста в последнем случае может быть больше.
Процессы метаболизма в клетках термофилов протекают с гораздо большей скоростью, чем в клетках мезОфилов. Поэтому концентрация растворенного в среде кислорода может явиться фактором, лимитирующим рост термофильных микроорганизмов. Однако при культивировании термофильных микроорганизмов на богатых естественных средах в условиях интенсивной аэрации организмы могут и не испытывать недостатка в растворенном кислороде. Но при выращивании термофилов на синтетических средах количество растворенного кислорода начинает выступать в роли решающего фактора.
Очень интересны опыты Р. Дж. Доунея. Этот исследователь показал, что при повышенной температуре необходимо насыщение среды кислородом под давлением, равным 1 атм. В этих условиях растворимость кислорода увеличивается. Так, при 60 °С концентрация кислорода была равна 139 микромолям, это значение близко к концентрации кислорода в среде для развития мезофильных форм при обычных температурах (143 — 240 микромолей). Выращивая Вас. stearothermophilus на полноценной питательной среде с повышенным содержанием кислорода при 60 °С, Доунею удалось получить большую биомассу этих бактерий. Таким образом, выяснилось, что биомасса клеток является функцией концентрации кислорода в среде и максимальное ее количество достигается при растворении кислорода в среде под давлением, равным 1 атм. Дальнейшее увеличение концентрации кислорода замедляет рост бактерий.
Процесс дыхания у термофильных микроорганизмов осуществляется гораздо интенсивней, чем у мезофилов. В лаборатории Л. Г. Логиновой был отмечен рштересный факт, ранее не описанный в литературе. При ускорении процесса дыхания с повышением температуры культивирования в клетках термофильных микроорганизмов заметно увеличивалось количество цитохромов. Особенно значительно оно возрастало в клетках облигатно-термофильных бактерий Вас. stearothermophilus, Вас. circu-lans, Вас. megaterium, Вас. brevis при температуре выращивания 65 °С. При этой температуре количество цитохромов возросло примерно в 2—2,5 раза по сравнению с их количеством в клетках бактерий, выращенных при температуре 55 °С.
Интересно отметить, что некоторое увеличение количества цитохромов при повышении температуры роста также наблюдалось и у мезофилов, но оно было значительно слабее, чем у термофильных форм микробов.
Потребность термофилов в питательных веществах зависит от температуры их роста. Л. Л. Кэмпбелл и Б. Пейс разделили по этому признаку термофильные спорообразующие бактерии на три группы. К первой группе относятся термофильные бактерии, потребность в питательных веществах которых не зависит от температуры. Бактерии второй группы нуждаются в дополнительном питании при повышении температуры выращивания, .а третьей группы — при понижении температуры.
Влияние аэрации – Условия развития и активности молочных бактерий вина
ФАКТОРЫ, ВЛИЯЮЩИЕ НА РАЗВИТИЕ МОЛОЧНОКИСЛЫХ БАКТЕРИЙ
Углеродное питание. Молочнокислые бактерии используют незначительные количества тех соединений, которые служат источником энергии. Основным источником энергии для молочнокислых бактерий являются моно- и дисахариды — глюкоза, лактоза, сахароза, мальтоза.
В качестве источника энергии и в конструктивном обмене они используют и органические кислоты — лимонную, яблочную, пи-ровиноградную, фумаровую и др. L. brevis в качестве источника углерода могут использовать уроновые кислоты — глюкуроно-вую и галактуроновую с образованием СО2, уксусной и молочной кислот [73]. В отсутствие сбраживаемых углеродсодержащих субстратов молочнокислые бактерии в качестве источника энергии утилизируют аминокислоты (глутаминовую кислоту, аргинин, тирозин), декарбоксилируя их с выделением С02. Полисахариды, как правило, молочнокислые бактерии не используют.
Многие молочнокислые бактерии нуждаются при развитии в наличии СО2, который они употребляют для биосинтеза белков, жирных кислот и др.
Азотное питание. По потребности в источниках азота молочнокислые бактерии можно разделить на три основные группы: нуждаются в сложном комплексе аминокислот (подрод Thermobacterium) ;
хорошо развивающиеся на цистеине и аммонийных солях (подрод Streptobacterium);
могут развиваться на аммонийных солях в качестве единственного источника азота (подрод Streptococcus).
Поскольку значительное число молочнокислых бактерий не способно синтезировать сложные органические формы азота, им необходимы питательные среды со сложными органическими формами азота — смесями аминокислот, гидролизатами белков (мяса, казеина, муки фасолевой, соевой, виковой), являющимися источниками пептонов, пептидов, различных аминокислот.
Витамины. Для развития молочнокислых бактерий, особенно для палочковидных форм, витамины являются необходимыми факторами [73].
Установлено, что все виды палочковидных бактерий нуждаются в пантотеновой кислоте, биотине, никотиновой кислоте, а гетероферментативные—еще и в тиамине. Не требуется им инозит, холин и n-аминобензойная кислота.
Количество пиридоксина (витамина В6), необходимое для развития молочнокислых бактерий, зависит от качественного и количественного аминокислотного состава среды, что является свидетельством определенной функции витамина Вб — катализ синтеза необходимых им аминокислот.
При наличии в среде олеиновой кислоты у L. fermenti утрачивается потребность в биотине [21].
Е. И. Квасников и О. А. Нестеренко, используя полную питательную среду, изучили большую коллекцию штаммов молочнокислых бактерий и установили зависимость между потребностью в витаминах и видовой принадлежностью штаммов.
Следует обратить внимание на то, что потребность молочнокислых бактерий в отдельных витаминах может изменяться от присутствия тех или иных аминокислот, жирных кислот и дезок-сирибозидов. Пуриновые основания влияют на потребность бактерий в n -аминобензойной кислоте; потребность в фолиевой кислоте значительно снижается, если используют среду, содержащую все известные аминокислоты, тимин (или тимидин) и пуриновые основания, которые синтезируются бактериями при участии фолиевой кислоты.
В винах витамины содержатся в количествах, необходимых для развития молочнокислых бактерий. Потребность молочнокислых бактерий в витаминах показана в табл. 40 [315].
Отчетливую стимуляцию роста молочнокислых бактерий, кроме аминокислот и витаминов, вызывает олеиновая кислота (до 4 мкг/мл), а также линолевая и линоленовая, которые могут заменять олеиновую кислоту; уксусная (до 40 мкг/мл) и лимонная кислоты; тимидин (до 2 мкг/мл) [21]. Для роста некоторых бактерий эффективны вещества с высокой восстановительной способностью, такие, как глутатион, аскорбиновая кислота [73].
Иногда пептиды стимулируют рост клеток молочнокислых бактерий более эффективно, чем свободные аминокислоты, к примеру, гистидиновый пептид по сравнению с гистидином.
Неорганические соединения. Для развития молочнокислых бактерий необходимы неорганические соединения — медь, железо, натрий, калий, фосфор, йод, сера, магний, марганец. Особенно важен марганец, который предохраняет клетки от автолиза [73].

Бактерии-кислотопонижатели нуждаются в присутствий комплекса минеральных веществ. Гетероферментативные кокки не развиваются в средах, лишенных путем ионообмена катионов металлов. Рост бактерий может быть вызван добавлением ионов К+ совместно с ионами Mg2+ или М g 2+. При содержании в среде Na+ совместно с К+ рост молочнокислых бактерий усиливается, в отсутствие ионов К+ усиление роста ион Na+ не вызывает. Ион М g 2+ расщепление яблочной кислоты увеличивает в 4 раза, Мg2+— на 50%.
Отмечено [333] положительное влияние на яблочно-молочное брожение стимуляторов роста, содержащихся в томатном соке. Наличие этого рода стимуляторов обнаружено и в других плодах и винограде, в красном больше, чем в белом, а в кожуре больше, чем в мякоти. Для выяснения природы этого фактора томатный сок был разделен физико-химическими способами на фракции. Исследования показали, что М g оказывает такое же влияние, как томатный сок, и его заменяет. Из 71 штамма бактерий 63 нуждались в добавлении к основной среде томатного сока или иона М g . Несмотря на несомненно стимулирующее влияние такого рода активаторов внесение их в вино вряд ли желательно, так как нарушает его натуральное сложение. Для стимуляции яблочно-молочного брожения могут быть применены приемы, свойственные технологическому процессу виноделия.
Кислород. Молочнокислые бактерии в отличие от аэробных, цитохромсодержащих, не имеют цитохромов, участвующих вдыхании, но они осуществляют активное окисление некоторых ве-174 ществ благодаря наличию флавопротеидных систем [51, 73]. Процесс окисления у молочнокислых бактерий часто связан с образованием перекиси водорода, подавляющей окисление. А некоторые из них могут вести процесс дальше, восстанавливая перекись до воды в присутствии окисляемых субстратов [335]. Максимум образования перекиси водорода наблюдается в логарифмической фазе роста культуры.
Отношение видов молочнокислых бактерий к аэрации среды различно и иногда противоположно., Так, строгий анаэробиоз, как правило, замедляет только начало развития гетероферментативных палочек; рост же гомоферментативных палочек явно снижает на 10%, а брожение на 23% [295]. Из кокковых форм, относящихся к гетероферментативным (Leuc. oenos), сбраживающие арабинозу достигают оптимального роста в анаэробных условиях, тогда как формы, не усваивающие пентозы, очень плохо развиваются в этих условиях [315].
Температура. В качестве основного критерия при классификации используется рост при температуре 15°С или при 45°С. Бактерии, изолированные из вин, не термофильны, не развиваются при температуре 45°С. Некоторые штаммы гомоферментативных молочнокислых бактерий могут развиваться при температуре 40°С в первые сутки. Оптимальной для развития молочнокислых бактерий признана температура 25°С. Однако кокковые формы в общем менее чувствительны к температуре, чем бактерии, и могут хорошо развиваться при температуре от 15 до 25°С. Результаты практики подтверждают эти сведения, поскольку яблочно-молочное брожение происходит при температуре 15°С и несколько медленнее при 10—12°С.
Спирты. Спирты обладают бактерицидным и бактериостатическим действием. Наибольшее бактерицидное действие этилового спирта наблюдается при концентрации 60—75% об.
Е. И. Квасниковым [69] и Э. О. Петян [137] изучено отношение к спирту нескольких тысяч штаммов молочнокислых бактерий как свежевыделенных из различных природных и производственных субстратов, так и коллекционных. Значительное количество штаммов молочнокислых палочковидных бактерий развивалось при концентрации этилового спирта (в % об.) 15—18, некоторые при 20 и 22 и даже при 24. Более низкие концентрации этилового спирта — 12—16% об. были предельными для кокковых форм.
Таким образом, приспособленность молочнокислых бактерий к развитию при высоких концентрациях этилового спирта является характерным свойством, присущим как гомо-, так и гетероферментативным формам. Так, из больных вин (сухих столовых и десертных) были выделены штаммы L. buchneri, которые развивались при содержании спирта 16—22% об. Значительной (до 23—25% об.) спиртоустойчивостью обладали штаммы, выделенные из резервуарного шампанского [67, 68]. Однако максимальная устойчивость к спирту проявляется на полноценных питательных средах, богатых аминокислотами и витаминами, и, наоборот, устойчивость к спирту значительно снижается на неполноценных питательных средах. Обогащение среды автолизатом дрожжей повышает спиртоустойчивость молочнокислых бактерий. Устойчивость бактерий к спирту также повышалась на 2% об. при длительном культивировании их с винными дрожжами.
Максимальное содержание эт илового спирта в среде,
Спиртоустойчивость молочнокислых бактерий, % штаммов
Источники:
http://vinograd.info/knigi/teoriya-i-praktika-vinodeliya/usloviya-razvitiya-i-aktivnosti-molochnyh-bakteriy-vina.html
http://studopedia.ru/3_132401_vliyanie-aeratsii-i-peremeshivaniya-na-rost-i-razvitie-aerobnih-termofilnih-bakteriy.html
http://sinref.ru/000_uchebniki/05599_vinodelie/020_mikrobiologia_vinodel/043.htm





