Техника экспериментирования – Коллоидные явления в винах
Техника экспериментирования – Коллоидные явления в винах
Электрокинетические явления в коллоидных системах;
Электрические свойства дисперсных систем
Лекция 7
ОПТИЧЕСКИЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
Лекция 6
B коллоидных растворах на границах раздела фаз возникают электрические заряды. Для понимания электрических свойств коллоидно-дисперсных систем необходимо изучение электрокинетических явлений в них, которые связаны с взаимодействием коллоидов с электролитами и наблюдаются при движении одной фазы относительно другой.
Электрокинетические явления в коллоидно-дисперсных системах и связанное с этими явлениями наличие электрических зарядов у коллоидов открыл Ф. Ф. Рейсс (1808). B опытах Рейсса в кусок влажной глины 1 (рис.1) были вставлены две стеклянные трубки 4, 5. B полученные таким способом цилиндры с глиняным дном насыпали хорошо промытый кварцевый песок 2 и налили в них до одинакового уровня воду. Опустив в цилиндры электроды от вольтова столба — одного из немногих известных в то время источников электрической энергии, включали ток. Через некоторое время под влиянием электрического поля частицы глины, отрываясь от поверхности, стали проходить сквозь песок и двигаться к положительному полюсу (аноду). Следовательно, эти частицы имели отрицательный заряд. B цилиндре с положительным электродом образовалась хорошо заметная суспензия (муть) 3. Одновременно уровень воды в цилиндре с отрицательным электродом (катодом) поднялся, а в цилиндре с положительным электродом опустился, что свидетельствовало о положительном заряде воды.

Рис. 1. Схема установки для проведения электрофореза.
При дальнейшем изучении этих явлений обнаружилось, что они характерны для коллоидно-дисперсных систем. Движение частиц дисперсной фазы в электрическом поле к противоположно заряженному электроду получило название электрофореза.
Пытаясь определить причины поднятия уровня воды в цилиндре с отрицательно заряженным электродом, Рейсс поставил другой опыт. Он пропускал постоянный ток через прибор, состоящий из И-образной трубки (рис.2), средняя часть которой была заполнена мелким кварцевым песком. B этом приборе кварцевый песок играл роль пористой диафрагмы. После включения электрического тока уровень воды в колене с отрицательным электродом начал повышаться, а в колене с положительным электродом — понижаться. Это продолжалось до тех пор, пока разность уровней в обоих коленах не достигла определенной величины. Многочисленные опыты показали, что, как и при электрофорезе, этот процесс протекает с постоянной скоростью. Причем количество перенесенной жидкости находится в прямой зависимости от приложенной разности потенциалов и диэлектрической проницаемости и обратно пропорционально вязкости этой среды. Впоследствии явление переноса жидкости через пористые диафрагмы и узкие капилляры получило название электроосмоса.

Рис. 2. Схема установки для проведения электроосмоса: 1 — И-образная трубка; 2 — кварцевый песок; 3 — вода
Позднее были открыты еще два электрокинетических явления, противоположные (по движению фаз) электрофорезу и электроосмосу.
Так, Kвинке (1859) обнаружил, что при механическом проталкивании воды через пористую диафрагму или через капилляр (что можно осуществить, применяя давление) на противоположных сторонах этой диафрагмы (или на концах капилляра) появляется разность потенциалов, препятствующая протеканию жидкости. Это явление получило название эффекта протекания или эффекта истечения, а возникающая разность потенциалов — потенциала протекания.
B 1878 г. Дорн обнаружил другое электрокинетическое явление, которое заключалось в возникновении скачка потенциалов при механическом передвижении твердых частиц в жидкой фазе (в опытах Дорна — при оседании крупинок песка в воде). Указанное явление обратно электрофорезу и получило название эффекта седиментации, а возникающий скачок потенциала — потенциала седиментации.
Таким образом, приложенная извне э.д.с. вызывает движение фаз: 1) электрофорез, если в движение приходит твердая фаза по отношению к неподвижной (в целом) жидкой фазе; 2) электроосмос, если приходит в движение жидкая среда по отношению к неподвижной твердой фазе. Механическое передвижение фаз, со своей стороны, вызывает э.д.с.: 1) потенциал седиментации, если сообщается движение твердой дисперсной фазе по отношению к неподвижной жидкой; 2) потенциал протекания, если сообщается движение жидкой фазе по отношению к неподвижной твердой фазе (поверхности).
Явления электрофореза и электроосмоса широко используются в технике и производстве. Электрофорез применяется в фарфоровом производстве для выделения из суспензий глин чистого каолина. Наиболее мелкие отрицательно заряженные частицы каолина после тщательного взмучивания в воде осаждаются на вращающемся свинцовом барабане, заряженном положительно. Посторонние примеси в виде положительно заряженных частиц Fе2О3, а также более крупные частицы каолина уносятся проточной водой. С помощью электрофореза различные изделия покрывают тонким слоем каучука из латекса. При этом отрицательно заряженные частицы латекса движутся в электрическом поле к аноду (покрываемый предмет) и осаждаются на нем. За последние годы метод электрофореза нашел широкое применение в получении оксикатодов в радиолампах.
Очень большое распространение получил метод инженера Kоттреля с применением электрофореза в борьбе с топочными дымами и производственными пылями, а также для улавливания в заводских трубах наиболее цепных отходов производства. B заводских трубах устанавливают специальные металлические стержни, на которые подается отрицательное напряжение (в десятки тысяч вольт). Частицы дыма и пыли имеют одноименный заряд со стержнем и отбрасываются от него с силой на поверхность трубы. Аналогичным способом очищаются газы всевозможных примесей.
Методы электроосмоса применяются в фильтр-прессах для обезвоживания различных пористых материалов, например торфа, а также для пропитки пористых материалов (например, древесины). B последние годы электроосмос довольно широко применяют для понижения уровня грунтовых вод, а также для осушения грунтов, особенно глинистых, в анодной зоне.
Электроосмос применяется также при производстве кирпича для смачивания проволоки, режущей глиняные заготовки. При этом проволоку соединяют с отрицательным, а брусок глины — с положительным полюсом.
Коллоидные явления в винах – Работы последнего времени
Содержание материала
Эта книга была отредактирована, когда появились публикации важных работ по исследованию фильтрации и прозрачности вин, состоянию белков и коллоидов углеводной природы в суслах и винах. Поэтому ниже приведены только ссылки на эти недавно выполненные работы с указанием на наиболее существенные моменты их содержания.
Исследование прозрачности
Изучение прозрачности вин, ее. сущности, ее определения и эффективности различных способов, проводимых для осветления, стало объектом конвенции под названием «Научное исследование и разработка лучших кондиций и лучшего вида вин высокого качества». В ближайшее время она появится в виде отчета с большим количеством важных приложений.
В конвенции предусматривается возможность изменения условий работы: а) контроль эффективности технологических линий розлива вина и гигиены используемых материалов и оборудования; б) разработка наилучших условий предварительного осветления; в) распространение фильтрации на целлюлозно-асбестовых пластинах без каких-либо последствий для вкусовых характеристик вин и с возможностью уменьшения доз сернистого ангидрида. В этой работе участвовали Мандро, Пейно, Серрано, Гимберто, Ловно и П. Риберо-Гайон. Краткое содержание результатов будет дано в томе 4 настоящей книги.
Исследование белков сусла и вина
По этому вопросу Фейлат (1974) написал докторскую диссертацию, в которой исследуются: а) влияние обработок мезги до брожения на содержание аминокислот; б) новые способы анализа белков и пептидов — методика анализа, основанная на сочетании различных физических методов разделения: ультрафильтрации, хроматографии на геле структурированного декстрана (Сефадекс), электрофорезе на полиакриламидном геле, хроматографии на ионообменниках.
Хотя в предыдущем разделе публикации Фейлата (1970, 1972, 1973) были изложены в общих чертах, в тезисах более точно и детально описаны полученные результаты. В частности, белковая фракция составляет только от 5 до 10% общего азота и состоит на 60— 70% из молекул с массой, близкой к 8000, несомненно, из тех, которые были названы полипептидами в предыдущей работе Фейлат (1973). С другой стороны, белки и пептиды представляют собой стабильные фракции во время брожения, так как они не усваиваются дрожжами и к тому же протеазы винограда быстро ингибируются спиртом.
Исследование коллоидов полисахаридной природы
В разделе «Разделение и идентификация коллоидов вина электрофорезом» дан анализ предыдущих работ Усельо-Томасет (1963, 1974) по этому вопросу. В 1975 г. этот же автор сообщил о современном состоянии его исследований, опубликовав работу «Растворимые коллоиды полисахаридной природы в суслах и винах»; здесь он снова применяет самые разнообразные методы анализа.
В качестве цели автор поставил себе определение специфической характеристики и количества различных мономеров, которые можно получить гидролизом коллоидов. Прежде всего, он сообщает о приоритете и важности работ Бюхи и Дойеля, которые осаждали спиртом коллоиды из 400 л центрифугированного сусла и пришли к выводу, что независимо от пектинов (выделенных в виде пектата кальция после щелочного гидролиза) коллоидное вещество является гомогенным и состоит из одного вида коллоида, хотя и сложного, содержащего галактуроновую кислоту, галактозу, маннозу, арабинозу, рамнозу, тогда как глюкоза и ксилоза отсутствуют.
К этому перечню мономеров, встречающихся в осаждаемых коллоидах сусел, Усельо-Томасет добавляет гликуроновую кислоту. С другой стороны, он установил, что молекулярные массы у 60—70% коллоидов сусел и вин находятся между 20 000 и 200 000; менее 5% коллоидов имеют молекулярную массу более 500 000 или менее 6500. Автор делает вывод, как и Бюхи и Дойель, о существовании одного сложного (комплексного) коллоидного вещества.
ЗАКЛЮЧЕНИЕ
На многие вопросы еще нет ответа не только из-за недостаточно глубокого знания коллоидных структур, но также из-за влияния различных видов коллоидов на фильтруемость, осаждение малорастворимых солей, на стабилизацию вин. Недавние работы в этом направлении представляют определенный вклад в разработку способов, обеспечивающих продолжение более глубоких исследований этой сложной и трудной проблемы.
В области коллоидов вина, как и в любом другом разделе энологии и как в любой отрасли науки, методы исследования усложняются по мере научного прогресса. Получение новых результатов становится все более и более трудным делом. Безусловно, что в технологии производства и хранения вин могут применяться только прогрессивные способы. Авторы считают, что перед энологией стоят проблемы, относящиеся к коллоидам и коллоидным явлениям, которые являются наиболее важными, актуальными и трудными для разрешения.
В этой главе, посвященной коллоидным явлениям в винах, авторы по необходимости рассматривали частицы в более или менее прозрачном коллоидном растворе и частицы, флокулированные или находящиеся в процессе флокуляции, которые вызывают или усиливают помутнения вина. Экспериментальные способы должны обеспечивать исследование различных состояний коллоидов, измерение степени помутнения, подсчет взвешенных частиц. Такие способы могут применяться и в тех случаях, когда мутность не является результатом коллоидных процессов, если она, например, связана с присутствием инертных частиц во взвешенном состоянии или с- развитием микроорганизмов, дрожжей и бактерий. Поэтому некоторые разделы этой главы будут использованы и в отдельных случаях дополнены в первой части тома 4, названной «Осветление и стабилизация».
Коллоидные явления в винах – Обзор общих сведений о коллоидах
Содержание материала
ОБЗОР ОБЩИХ СВЕДЕНИЙ О КОЛЛОИДАХ
Классификация дисперсных систем
Дисперсными системами, или дисперсиями, называют системы, составленные из какого-либо вещества, рассеянного в другом, в частности в жидкости, в состоянии тончайших частиц. Коллоидные дисперсии представляют собой системы, в которых вещество рассеяно в жидкости в состоянии крупных агрегатов маленьких молекул (или мицелл) или в состоянии больших молекул (или макромолекул), другими словами, в состоянии частиц определенных размеров — от обычных молекул до взвешенных частиц. Но классификация дисперсных систем по размерам частиц подходит только для частиц хотя бы приблизительно сферической формы и не годится для частиц удлиненной формы, как это часто бывает в органических коллоидах.
Таблица 11.1
Классификация дисперсных систем
Размеры частиц, им
Число атомов в одной частице
Молекулярные дисперсии (или ординарные растворы)
Приблизительно менее 2
Проходят через бумажные и ультрафильтры; не видимы в. микрсскоп и в ультрамикроскоп; диффундируют и диализуются, не осаждаются
Коллоидные дисперсии (или растЕоры). Частицы могут быть микрокристаллами, макромолекулами
Приблизительно от 2 до 100
Между 1000 и 1 000 000 000
Проходят через самый плотный, бумажный фильтр, но не проходят через ультрафильтры; не видимы в микроскоп, но в ультрамикроскопе видны, не диффундируют и не диализуются, осаждаются очень медленно
Грубые дисперсии (или суспензии)
Приблизительно более 100
Свыше
1 000 000 000
Не проходят через бумажный, фильтр, видны в микроскоп, не диффундируют и не диализуются; оседают очень быстро
Указанные в табл. 11.1 пределы таких систем имеют производственный характер и не определяют ни конца одного вида частиц, ни начала другого. Между этими видами нет точных, определенных разграничительных линий: виден непрерывный переход между истинными растворами, коллоидными и суспензиями. Признаки, указанные в последней графе табл. 11.1, зависят одновременно от рассматриваемых веществ и технических условий, таких, как природа диализующей мембраны, размеры пор фильтров и разрешающие способности микроскопа. Известна целая гамма дисперсных систем, или гетерогенных растворов, и в этой шкале дисперсии, или коллоидные растворы, перемежаются с молекулярными растворами и суспензиями. Коллоидные свойства достаточно охарактеризованы только в центральной зоне коллоидных дисперсий с пределами, которые могут изменяться в зависимости от природы частиц.
Согласно Крюйти и Овербику (1961), коллоидные системы имеют частицы, размеры которых находятся в пределах от 1 до 1000 нм.
К группе коллоидов, способных образовывать коллоидные дисперсии, относят очень различные вещества, не имеющие никакой связи между собой по происхождению или составу (простые или очень сложные органические вещества), но которые имеют некоторые общие свойства. В этом отношении также нет четко обозначенной границы между коллоидами и неколлоидами (или «кристаллоидами», как говорили раньше). Некоторые вещества имеют в зависимости от условий те или иные свойства. Например, хлористый натрий и многие другие соли дают с водой истинные, или молекулярные растворы. Но при более или менее значительном добавлении спирта они дают коллоидные растворы со всеми степенями дисперсий, промежуточных между молекулярным раствором и осадком. Точно так же и фенольные соединения могут быть в истинном растворе или в коллоидном.
В качестве примера можно, сказать, что глины, такие, как каолин и бентонит (которые используются для обработки вина), образуют в воде мутные суспензии, размеры частиц которых значительно больше, чем у коллоидных гранул, вплоть до 2 мкм. Но в действительности эти гранулы образуются из частиц кремния и алюминия, наложенных одна на другую на расстоянии (примерно 1 нм), соответствующем точно величине коллоидных частиц. Жидкость проникает в промежуток между частицами и обменивается с ними некоторыми из своих компонентов. Эти обмены происходят намного легче у монморилонита, чем у каолинита, частицы которого намного больше сближены и связаны между собой. Можно сказать, что коллоидные свойства выражены в большей степени у монморилонита, который поглощает много воды, сильно набухает и фиксирует много ионов из раствора. По своим свойствам он ближе к гидрофильным коллоидам, тогда как каолинит ближе к гидрофобным коллоидам.
Основные понятия
Терминология науки о коллоидах и коллоидных явлениях все еще неточна, и значения отдельных терминов изменяются в зависимости от автора. Ниже будут упоминаться такие термины и выражения, которые, по мнению авторов настоящей книги, лучше всего подходят для описания и объяснения коллоидных явлений, встречающихся в энологии.
Как правило, коллоиды могут находиться в состоянии коллоидных растворов (называемых также золями, или псевдорастворами) или в состоянии гелей. Золь обладает текучестью, небольшой вязкостью, не затвердевает; частицы не связаны одна с другой и находятся в спонтанном, беспорядочном движении, называемом броуновским, которое вызывается столкновением соседних молекул. Гель, наоборот, характеризуется тем, что в этом состоянии частицы неподвижны одна относительно другой, группируются в более или менее крупные скопления. Такие связи препятствуют броуновскому движению. Гель обладает жесткостью и гибкостью и ведет себя, как настоящее твердое тело. Он состоит из ткани, которую можно сравнить с сеткой взаимно переплетающихся фибровых нитей и ячеек, наполненных жидкостью. Желе (или гелем, студнем) называют аморфные вещества, (желатина, крахмал, агар, каучук и др.), которые набухают при погружении в соответствующую жидкость.
Под пептизацией понимают переход коллоида из состояния геля в состояние золя. Этот процесс можно сравнить с растворением геля. Флокуляция означает переход из состояния золя в состояние геля. Ее можно сравнить с осаждением соли; частицы, первоначально свободные, слипаются и стремятся выйти из жидкости, образуя хлопья, являющиеся кусками геля. Термин «осаждение» означает всякое отделение растворенного вещества от растворителя в любой форме; тонкий осадок, кристаллизованный или нет, большего или меньшего объема, делающий жидкость мутной, или оседающей, видимый на глаз. В случае коллоидов этот термин часто используют в том же смысле, что и термин «флокуляция». Под термином «коагуляция» понимают переход из состояния золя в состояние геля; частицы агломерируются внутри жидкости, но не в отдельные хлопья, как при флокуляции, а в одну сплошную массу; происходит охватывание коллоида без разделения на две фазы, как при флокуляции. Термин «синерезис» означает переход из состояния желе в состояние геля. Масса коллоида претерпевает сжатие, сокращается в размерах с выталкиванием большей части инертного вещества, который находился в желе, следовательно, желе дает две фазы.
Схема, изображенная на рис. 11.1, дает представление об изложенных: выше определениях. 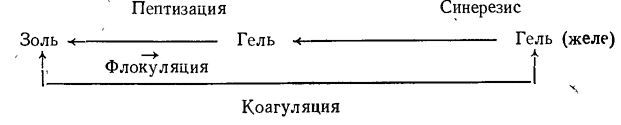
Рис. 11.1. Схема коллоидных превращений.
Флокуляция есть не что иное, как сумма коагуляции и синерезиса: сначала происходит застудневание, затем ослабление этого желе в результате разрыва и контрактации его сетки. Хлопья геля всего лишь обломки, куски этой разрушенной массы, которая выталкивает растворитель с одновременным сокращением своего объема. Многие гели в действительности представляют собой желе, набухшее до крайних размеров; они как бы разламываются от чрезмерного разбухания, поскольку внутренние связи оказываются недостаточно прочными. Фактически при оклейке вин коагуляция и синерезис могут в некоторых условиях протекать совершенно раздельно: сначала затвердевание (схватывание), затем разрыв массы путем перемешивания.
Другие авторы применяют названия гель и желе, флокуляция и коагуляция в более или менее различном смысле. Некоторые применяют только термины «гель» и «осаждение»; при этом гель означает все состояния, в которых коллоид находится в более или менее твердом, эластичном, жестком состоянии, а осаждение означает все разделения коллоида и жидкости. В исследовании по оклейке вин удобно использовать термин «флокуляция» для обозначения осаждения в форме видимых на глаз хлопьев, которое обычно» сопровождается осаждением хлопьев и осветлением жидкости. К тому же флокуляцией в просторечии называют «осаждение некоторых коллоидных растворов в виде хлопьев». Такая неопределенность терминов ведет к неправильным представлениям о сложной структуре гелей и желе.
Источники:
http://studopedia.su/4_7195_elektrokineticheskie-yavleniya-v-kolloidnih-sistemah.html
http://vinograd.info/knigi/teoriya-i-praktika-vinodeliya/kolloidnye-yavleniya-v-vinah-18.html
http://vinograd.info/knigi/teoriya-i-praktika-vinodeliya/kolloidnye-yavleniya-v-vinah-2.html





