Работы последнего времени об окислительно-восстановительных процессах в винах – Процессы окисления и восстановления в винах
Работы последнего времени об окислительно-восстановительных процессах в винах – Процессы окисления и восстановления в винах
Работы последнего времени об окислительно-восстановительных процессах в винах – Процессы окисления и восстановления в винах
Здравствуйте Игорь. Внимательно прочитал про окисление вина. Но так толком и не понял. Стоит ли пугаться в домашнем виноделии этой «страшилки»?
Как то описали вы это, прошу прощения, обтекаемо: окисляется…теряет ароматы..серу надо. А конкретики нет, т.е. главного.
1. Когда начинается заметное окисление стабильного вина?
2. Всегда ли присходит окисление вина?
3. Если не всегда, то в каких случаях, как правило, начинается?
4. За кокое время процесс окисления превращает вино в «помои»?
5. Так ли необходима сера в вине, то бишь сульфатация?
Хотелось бы, если не в напряг, получить от вас ответы на вопросы.
С уважением, Валерий Васильевич
Валерий Васильевич,
Вы либо не пили окисленного вина, либо не пили НЕокисленного (скорее всего), раз задаёте такие вопросы, и оно Вас полностью устраивает.
Данная статья размещена в разделе авторского виноделия, т.е. для подготовленных читателей. Вам нужно для начала внимательно изучить все статьи (с комментариями) раздела о домашнем виноделии.
Вы хотите чтобы я Вам описал вкус? Найдите возле Вас более опытного винодела, пусть он Вам с бокалом в руках покажет окисленное вино.
Окисление вина происходит всегда, в продолжение всей его жизни, на каком-то этапе это нам на пользу, а с определённого — во вред. Точно, о конкретной скорости процесса, можно говорить только в приложении к конкретному вину, конкретной ситуации.
А про добавление серы в вино у меня здесь написано предостаточно. Ищите. Направления я Вам уже показал («Домашнее виноделие»).
Игорь, в заключении вы пишете:-«Понимание химизма процессов окисления вина сильно развилось за последние 10-20 лет…»
А до этого, пока понимание химизма не развивалось, все пили окисленное вино?
Вино ведь существует сколько существует человек.
А химизм?
Вам не кажется, что происходит просто, можно сказать бездумный, процесс переноса промышленной технологии на процесс домашнего виноделия?
Мне кажется, что я читаю сообщения человека, абсолютно не понимающего, о чём идёт речь.
Сколько можно повторять, что это раздел для подготовленных читателей, «Авторского», а не «Домашнего», виноделия.
Выучите арифметику, прежде чем рассуждать о дифференциальных уравнениях. В теме о домашнем виноделии, как минимум.
И соблюдайте вложенность («лесенку») комментариев.
Игорь Владимирович, здравствуйте! А Вы не могли бы подсказать, как можно понизить кислотность сусла. Из-за повышенной кислотности моего винограда, вынужден, добавлять сахар в вино. Получается очень вкусное и ароматное, но хочется и сухого.
Эмиль, Вы вообще статью прочли, которую комментируете? Неужели не увидели, что «окисление» и «кислотность» в виноделии есть понятия суть разные?!
Сыпаньем сахара в вино Вы не понизите его кислотность, количество кислоты в вине не изменяется. Гуглите «методы понижения кислотности сусла (вина)». Разбавление, калинат и т.п. Вам в помощь.
Игорь Владимирович,доброго времени!
Прошлогоднее вино не сульфитировал стоит в подвале под пробкой,как я понимаю через туже пробку и окисляется.Есть мысль разбавить прошлогоднее вино,с вином этого года, чрезмерно сульфитированным,для стабилизации прошлогоднего?
И ещё если можно вопрос.Как отличить спиртовое брожение, от уксусного не дожидаясь окончания этого самого брожения?
Игорь Владимирович! Или так хранить?Вино сухое кисловатое,но аромат.
Этот аромат заставляет меня совершенствоваться и докучать вас своими вопросами.Спасибо за ваши ответы!
Здравствуйте, Игорь. Огромное спасибо за Ваши труды. Подскажите пожалуйста, на каком этапе приготовления вина вносится аскорбиновая кислота ? Cпасибо еще раз.
В самом начале — при дроблении винограда, и перед розливом.
Процессы окисления и восстановления в винах – Окислительно-восстановительные процессы и вкусовые характеристики вин
Содержание материала
Общие замечания. Если действие кислорода в первый период созревания необходимо, то в дальнейшем он играет намного меньшую роль и даже оказывает явно отрицательное влияние на качество белых вин. Можно предполагать, что при осторожной аэрации, которая бывает при хранении вина в деревянных бочках, окисление осуществляется при низком окислительно-восстановительном потенциале. Кроме того, при хранении вин в деревянных бочках окисление происходит в вине, находящемся в контакте с деревом и очень богатом дубильными веществами. Наконец, при старении вина в бутылках вообще не происходит каких-либо явлений окисления; наоборот, образование сложных эфиров и других продуктов букета идет в результате восстановления. В целом роль кислорода в созревании вина не столь исключительна, как это представлял Пастер. Кроме того, яблочно-молочное брожение является первым периодом созревания вин.
В данном разделе рассматриваются отношения между окислительными и восстановительными процессами, происходящими в вине, степенью окисления-восстановления его и развитием или потерей букета. Аэрирование вина за счет продолжительного контакта с воздухом или после растворения кислорода путем мгновенного контакта с воздухом влечет за собой появление более или менее выраженных признаков выветренности и других характеристик в зависимости от природы вина. Ароматические вещества изменяются или разрушаются, затем появляется горечь, связанная с присутствием свободного уксусного альдегида.
«Бутылочная болезнь» представляет собой особый случай потери букета вина. Когда вино снова лишают доступа воздуха, например в бутылках, признаки потери букета постепенно исчезают. Потом с течением времени появляются запахи, присущие винам, хранящимся без доступа воздуха. Именно в таких условиях полностью развивается букет красных и белых вин из тонких сортов, культивируемых на виноградниках, дающих продукцию высокого качества. Если вино, которое длительное время находилось в состоянии покоя, снова подвергнуть аэрации, то уже через несколько часов его букет изменяется или разрушается. Это не относится к типам вин, обладающих характеристиками ранчио или мадеры, которые связаны с постоянным состоянием окисления и с высоким содержанием ацетальдегида.
Нельзя все объяснить только одним прямым воздействием кислорода. Одно присутствие растворенного кислорода само по себе не вносит почти никаких изменений в органолептические качества вина вопреки тому, что думал Пастер. Вкус вина, дегустированного сразу же после насыщения его кислородом, не изменялся. Появление привкуса выветренности есть результат реакций, вызываемых кислородом в последующие часы. Кислород окисляет вещества вина, а при отсутствии воздуха они восстанавливаются.
Потенциал аэрированного вина равен примерно 400—450 мВ (что соответствует г.Н от 19 до 22). Потенциал вина, длительное время хранившегося без доступа воздуха, или предельный потенциал, равен приблизительно 100—150 мВ (что соответствует гН от 9до11).
Запахи и, в частности, тонкий букет, образующийся у вин лучших марок при старении в бутылках, обусловлены запахом веществ, которые приобретают свой приятный букет только в восстановленной форме. Образование букета есть не что иное, как процесс восстановления. Авторы уже заметили этот факт, но он еще нуждается в уточнении.
Условия образования букета. Развитие букета связано, по-видимому, прежде всего с присутствием особых ароматических веществ кожицы винограда тонких сортов, а также с постепенным уменьшением окислительно-восстановительного потенциала, которое продолжается и после исчезновения кислорода. Наконец, интенсивность букета оказывается связанной с достигнутым предельным потенциалом, который зависит от природы вина и эффективности обтюрирующего устройства, равно как и от температуры и Освещения.
В вине в бутылках интенсивность букета возрастает и параллельно уменьшается потенциал. Развитие букета также ускоряется газообразным водородом, который понижает потенциал на 240—450 мВ, что может повести к значительному улучшению букета.
Степень восстановления данного вина зависит от температуры. При незначительном повышении температуры содержание кислорода уменьшается быстрее, так же как и потенциал. Наоборот, букет вина усиливается быстрее, когда температура хранения повышена, но не превосходит некоторого предела (примерно 25°С), выше которого вино часто приобретает вкус пригорелости (особенно если оно подвергалось излишне сильному сульфитированию и имеет повышенную кислотность). Наибольшее развитие букет получает летом в течение нескольких лет подряд. На практике можно немного ускорить этот процесс у выдающихся вин (белых или красных), разлитых в бутылки, если хранить их при несколько повышенной температуре, избегая низких температур зимой и производя подогревание воздуха в помещениях.
Солнечный свет сильно ускоряет процессы восстановления, особенно в белых сульфитированных винах. Запах, напоминающий букет выдержки, но деформированный и неприятный, развивается еще до того, как будет израсходован весь кислород и будет восстановлено железо, и иногда даже несмотря на легкий контакт с воздухом. При солнечном освещении очень ускоряется развитие медного касса. Здесь может быть вмешательство спирта, который под действием солнечной радиации образует альдегид с восстановлением растворенных веществ.
В качестве примера можно указать на тот факт, что в белых винах, выставленных зимой на солнечный свет в течение двух месяцев, окислительно-восстановительный потенциал снизился до 115—160 мВ, тогда как эти же вина, хранившиеся в течение такого же срока в темноте в термостате при 23°С, имели потенциал от 160 до 240 мВ. В белых сульфитированных винах, хранящихся в бутылках на протяжении десятка лет, потенциал был от 100 до 130 мВ. Присутствие свободной сернистой кислоты понижает предельный потенциал.
Состояние восстановления для данных условий герметичности закрывания емкостей и хранения зависит от содержания сернистой кислоты, которая заметно повышает, как в красных, так и в белых винах скорость, с которой уменьшается потенциал и образуется букет. Для развития букета, свойственного некоторым белым винам лучших марок, требуется достаточное содержание свободной сернистой кислоты, например 50—60 мг/л.
Содержание металлических ионов, в частности ионов двухвалентной меди, играет важную роль в развитии букета красных и белых вин в бутылках. Добавление к белым сульфнтированным винам от 2 до 3 мг/л меди (в виде сульфата) препятствует развитию аромата или намного уменьшает его интенсивность. Обработка белых вин моносульфидом натрия, которая оставляет в вине лишь несколько десятых миллиграмма на 1 л меди, заметно усиливает развитие букета; напротив, добавление 1 мг/л меди к вину, обработанному таким образом, уничтожает в этом отношении эффект обработки.
Наконец, почти полное удаление меди желтой кровяной солью усиливает с одновременным ухудшением нормальный аромат белых и красных вин в бутылках. Вино приобретает несколько острый, пригорелый запах, напоминающий букет сульфитированных белых вин на солнечном свету, который усиливает явления восстановления. Отсюда следует, что присутствие в вине следов иона меди порядка одной десятой или нескольких десятых миллиграмма на 1 л, но не больше было бы полезным для развития букета.
Сообщали также, что в игристых винах при добавлении аскорбиновой кислоты в момент, когда производят дегоржаж, получают более тонкие вина с намного более низким редокс-потенциалом. Без аскорбиновой кислоты железо остается окисленным на неопределенно долгое время.
Состояние восстановления зависит от герметичности емкости. В бутылках вместимостью 750 см 3 , хорошо закупоренных пробкой высокого качества (плотной и мягкой во всех направлениях) при воздушной камере 5—10 см 3 или без нее, с колпачком или покрытием на горлышке или без них, получаются хорошие результаты.
С другой стороны, склянки вместимостью 125 или 180 см 3 , закупоренные обычным способом — пробкой с помощью укупорочной машины, ведут себя совершенно иначе, чем бутылки вместимостью 750 или 375 см 3 ; укупорка совершенно недостаточна; содержание сернистой кислоты заметно понижается; букет не развивается или развивается плохо. Бутылки, используемые для образцов вина, нужно закупоривать пробками большего размера и более длинными, чем отверстие горлышка, или же снабжать укупорочными колпачками типа «корона», когда собственно пробка покрывается изолирующим вкладышем для предотвращения попадания металла в вино через пробку. Системы навинчивающихся пробок, совершенно неудовлетворительных в первых опытах, в настоящее время улучшены и получают все более широкое применение. Они очень эффективны, когда закаточная машина хорошо отрегулирована и прокладка, обеспечивающая контакт с вином, имеет достаточную толщину и непроницаемость. Ниже приведены значения предельного окислительно-восстановительного потенциала, достигнутые одним и тем же белым сульфитированным вином после хранения в бутылках в течение четырех летних месяцев в различных условиях.
Полное исследование закупоривания в зависимости от качества и формы пробки, ее приготовления, внутренней формы горлышка бутылки было бы очень полезно.
Корковая пробка изменяется под действием вина, особенно если вина сульфитированы. Она становится рыхлой и больше не дает хорошего закупоривающего эффекта. С другой стороны, пробка может быть постепенно перфорирована насекомыми. Поэтому можно понять необходимость применения достаточно длинных пробок, чтобы обеспечить продолжительное хранение вин и. замену их через 20—30 лет. Наконец, необходимо отметить, что часто пробки сильно сжимаются плашками укупорочных машин, когда последние имеют неудачную конструкцию или сильно изношены. В результате получается плохое закупоривание, и с течением времени может появиться просачивание жидкости.
Основная трудность плотного закупоривания бутылок заключается в расширении объема жидкостей, который у них намного больше, чем у твердых тел, т. е. у бутылок. Коэффициент объемного расширения стекла 27-10-6; следовательно, увеличение вместимости бутылки (750 см 3 ) составляет около 0,02 см 3 на 1°С. Параллельно с этим происходит увеличение объема вина, содержащего 15% об. спирта, которое при повышении температуры от 2 до 15°С составляет 1,4 см 3 . Когда же температура повышается от 15 до 28°С, объем вина возрастает еще на 2,2 см 3 (на 1,7 см 3 для вин, содержащих 7% об. спирта).
Коэффициент расширения вина воз растает с повышением температуры и содержания спирта. Следовательно, когда бутылка наполняется полностью и закупоривается зимой, вино неизбежно выталкивается из бутылки в течение лета; затем в течение следующей зимы образуется заметная воздушная камера объемом в несколько кубических сантиметров.
нагревавшееся до 80°С в течение 4 ч
в бутылках вместимостью 750 см 3 , закупоренных пробкой
в флаконе, закрытом притертой пробкой
в флаконе вместимостью 125 см 3 , закрытом пробкой
в флаконе вместимостью 125 см 3 , закрытом парафинированной пробкой
в флаконе вместимостью 125 см 3 , закупоренном пробкой и помещенном в закрытую банку с пирогаллолом
в флаконе, снабженном навинчивающейся пробкой недостаточной герметичности
На практике кажется рациональным для возможно большего уменьшения контакта вина с внешней средой оставлять при розливе воздушную камеру от 3 до 4 см 3 зимой, соответствующую 5—7 мм по высоте, и от 1 до 2 см 3 — летом. К тому же таким путем можно избежать потерь, которыми нельзя пренебрегать, тем более что закупоривание бутылок, заполненных доверху, неизбежно влечет при этом ощутимую потерю жидкости.
Условия потери букета. Если развитие букета в вине без доступа воздуха связано с появлением восстановительных веществ, то потеря букета, наоборот, связана с образованием в аэрированном вине окисленных веществ, и оба эти изменения являются обратимыми. Потеря букета состоит прежде всего в присоединении нескольких десятых кубических сантиметра кислорода в 1 л вина, в исчезновении или изменении большинства элементов букета и аромата, природных или приобретенных. Затем происходит развитие характерных привкусов горечи и остроты, которые представляют собой переходную степень к характеристикам, появляющимся при более длительной аэрации: вкуса ранено у красных вин и вкуса мадеры у белых. Скорость такой потери букета при окислении возрастает очень быстро при повышении температуры. Например, один и тот же результат достигается за несколько дней при зимних температурах и за несколько часов—в летний период. Но, когда вино снова изолируют от доступа воздуха, эффект выветренности исчезает или ослабевает и тем быстрее, чем выше температура.
Простой кратковременный контакт с воздухом, который бывает при спуске вина, при розливе или при взятии образцов, в результате чего происходит растворение кислорода (даже если в очень малом количестве), вызывает уже через несколько часов первые признаки потери букета. Букет старых вин в бутылках восприимчив к следам кислорода и появляется только спустя значительное время после его исчезновения.
Основным признаком выветренных вин является присутствие ацетальдегида или его продуктов. Значение окуривания бочек, в которые переливают вино после спуска его, состоит в том, чтобы помешать высвобождению альдегида, вводя в жидкость сернистую кислоту, которая возмещает количество ее, подвергшееся окислению вследствие аэрации при спуске вина.
Розлив вина в бутылки непосредственно из бочек производят без сульфитирования. Известно, что после этой операции в винах, в частности в красных, всегда более бедных сернистой кислотой, чем белые, проявляется более или менее выраженная потеря букета, которая наблюдается в течение нескольких месяцев и которую называют «бутылочной болезнью». В винах массового потребления можно избежать этого неблагоприятного превращения, если перед розливом в бутылки добавить в вино от 20 до 30 мг/л сернистой кислоты (более значительное добавление, примерно 50—100 мг/л, вызвало бы изменение характеристик вина).
Даже если во время этой операции аэрирование протекает очень энергично, вино остается в дальнейшем почта таким же, как и неаэрированное. Можно также приблизить по времени розлив в бутылки к снятию с дрожжей, для того чтобы содержание сернистой кислоты еще оставалось достаточным для предотвращения «бутылочной болезни». Ее можно также в большой степени ослабить, осуществляя розлив без разбрызгивания под низким давлением или же погружая сосок разливочной машины на дно бутылки. Это же относится и к взятию проб для дегустации, и к декантации старых вин в бутылках, букет которых очень чувствителен к кислороду. Было бы интересно проводить эти операции с помощью сифона или под инертным газом, т. е. с предварительным вытеснением воздуха из бутылки углекислым газом- или чистым азотом.
Наличие ацетальдегида не дает достаточного объяснения всех вкусовых характеристик выдохшегося вина. Например, для красных сильно окисленных вин, содержащих 20 мг/л сернистой кислоты и всего 15 мг/л альдегида, требовалось для полного исчезновения окисленного привкуса и признаков потери букета добавление сернистой кислоты примерно 100 мг/л, т. е. больше, чем необходимо для присоединения альдегида. В развитии явления потери букета и в его характеристиках выступают другие процессы окисления, которые выражаются в увеличении окислительно-восстановительного потенциала вина; уточнение природы их представляет большой интерес. Из работ, проведенных Пауль, вытекает, что потеря букета у молодых вин является результатом образования хинонов, которые их денатурируют. Но Кильгофер не разделяет эту точку зрения.
Окислительно-восстановительные процессы
Окислительно-восстановительные процессы (ОВП) играют важную роль в жизнедеятельности организма, поскольку именно в процессах окисления происходит выделение и запас энергии, а восстановительные процессы связаны с биосинтезом белков, нуклеиновых кислот, полисахаридов в организме. Окислительно-восстановительные реакции – это реакции, идущие с переносом электронов и изменением степени окисления элементов.
ОВП состоят из двух одновременно протекающих и противоположно направленных процессов – окисления и восстановления. Окисление – это процесс отдачи электронов, в ходе которого происходит увеличение степени окисления элементов. Восстановление – это процесс присоединения электронов, в ходе которого происходит уменьшение степени окисления элементов. Окислитель – это вещество, атом которого принимает электроны, тем самым уменьшая степень окисления. Восстановитель – это вещество, атом которого отдает электроны, тем самым увеличивая степень окисления. ОВП подразделяются на три типа.
1. Межмолекулярные, в которых окислитель и восстановитель находятся в разных молекулах, например:
окислитель – Mn +7 , восстановитель – N +3 .
2. Внутримолекулярные, в которых окислитель и восстановитель находятся в одной молекуле, но являются разными элементами, например:
2KCl +5 O3 -2 = 2KCl -1 + 3O4 0
окислитель – Cl +5 , восстановитель – O -2 .
3. Диспропорционирования (самоокисления – самовосстановления), в которых окислителем является один и тот же элемент в одной и той же степени окисления, например:
3Cl2 0 + 6KOH = 5КСl -1 + KCl +5 O3 + 3H2O
окислитель – Cl 0 , восстановитель – Cl 0 .
В ходе окислительно-восстановительных процессов между частями системы происходит перераспределение зарядов. Возникающая разность зарядов между частями системы носит название потенциал. Существует несколько видов потенциалов, связанных с прохождением различных процессов.
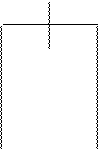
Одним из них является электродный потенциал, который возникает в том случае, когда пластинку металла погружают в раствор его соли (например, пластинку цинка в раствор сульфата цинка). При этом возможно прохождение двух процессов, которые определяются активностью металла и концентраций его катиона в растворе (рис.1).
 Ме Ме
Ме Ме
 + _ + _ _
+ _ + _ _

 Ме n+ + _ + Ме n+ _ + _
Ме n+ + _ + Ме n+ _ + _
 + _ + _ + _
+ _ + _ + _


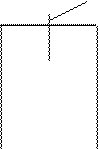
рис. 1 Виды электродных процессов
Первый процесс происходит в том случае, когда активность металла высока, а концентрация его катиона невелика. В этом случае (см. рис. 1) ионы металла, находящиеся в узлах кристаллической решетки металла, вследствие гидратации будут переходить в раствор, заряжая его положительно; электроны, входящие в состав «электронного газа» (особенности металлической связи) остаются на куске металла, придавая ему отрицательный заряд.
В случае низкой активности металла и высокой концентрации его катиона процесс может идти в другом направлении (см. рис. 2). Катионы металла могут перейти на пластинку, достраивая кристаллическую решетку металла и придавая ей положительный заряд; анионы соли остаются в растворе, заряжая его отрицательно. В обоих процессах между пластинкой металла и раствором его соли возникает разность зарядов, называемая электродным потенциалом Е. Независимо от механизма возникновения электродного потенциала, он определяется окислительно-восстановительным процессом, а его величина – уравнением Нернста:


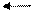
 Me Me n+ + ne –
Me Me n+ + ne –
 Zn Zn 2+ + 2e –
Zn Zn 2+ + 2e –
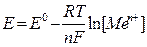
где: Е – потенциал системы,
Е 0 – стандартный потенциал системы, т.е. потенциал, определенный в стандартных условиях (Т=292 К, р=1 атм, [Red] = [Ох] = 1 моль/л)
Т – абсолютная температура,
n – число электронов, участвующих в процессе,
R = 8,31 Дж/моль * К,
F = 96500 Кл/моль
[Ме п+ ] – равновесная концентрация соли данного металла.
Подставляя постоянные при 25 0 С, получим:

По величине стандартного электродного потенциала все металлы выстраиваются в электрохимический ряд напряжений.
Одним из основных является окислительно-восстановительный потенциал. Его возникновение связано с обратимостью окислительно-восстановительных процессов. Одно и то же вещество в зависимости от условий может находиться либо в окисленной (Oх), либо восстановленной (Red) форме. Между этими двумя формами идут процессы взаимного перехода, сопровождающиеся изменением заряда системы. Процесс взаимного перехода идет до тех пор, пока между двумя формами не установится равновесие:

 Red Ox + ne
Red Ox + ne

 Fe 2+ Fe 3+ + e
Fe 2+ Fe 3+ + e
После установления равновесия в системе возникает избыточный заряд, называемый окислительно-восстановительным или редокс-потенциалом. Его величина определяется уравнением Нернста:
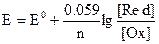
где: Е – потенциал системы,
Е 0 – стандартный потенциал системы, т.е. потенциал, определенный в стандартных условиях (Т=292 К, р=1 атм, [Red] = [Ох] = 1 моль/л)
[Red], [Ох] – равновесные концентрации восстановленной и окисленной форм.
Любой окислительно-восстановительный процесс можно представить как взаимодействие двух редокс-систем – системы окислителя и системы восстановителя. Направление ОВП будет определяться величинами редокспотенциалов систем.
При этом можно выделить следующие закономерности:
1. Одна и та же редокс-система может являться как окислителем, так и восстановителем – это зависит от соотношения величин потенциалов;
2. Системы с более отрицательным потенциалом будут восстанавливать системы с более положительным потенциалом;
3. После прохождения ОВП потенциалы редокс-систем выравниваются.
Возникновение разности зарядов между частями системы может быть и не связано с прохождением ОВП. Так, в ходе процесса диффузии между частями раствора, вследствие различной подвижности ионов, возникает разность зарядов, называемая диффузным потенциалом. Диффузный потенциал существует недолго и исчезает по окончании процесса диффузии.
Если два раствора разделить полупроницаемой мембраной, то на сторонах мембраны возникает разность зарядов, называемая мембранным потенциалом. Возникновение мембранного потенциала связано с тем, что вследствие различного размера ионов они могут проходить или не проходить через мембрану.
В живых организмах, вследствие наличия многочисленных мембран, направленного транспорта веществ и прохождения различных ОВП между его частями, возникает разность зарядов, называемая биопотенциалами. По своей природе биопотенциалы могут быть диффузными, мембранными и редокспотенциалами. Биопотенциалы играют важнейшую роль в направленном транспорте веществ, работе мембранных систем, процессах биосинтеза, выделение и запасание энергии. Выделение и запасание организмом энергии тесно связано с процессами окисления и восстановления.
77.243.189.108 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Источники:
http://www.zaika.in.ua/vinodelie/avtorskoe-garagnoe-vinodelie/okislenie-i-ego-vliyanie-na-aromat-vina/
http://vinograd.info/knigi/teoriya-i-praktika-vinodeliya/processy-okisleniya-i-vosstanovleniya-v-vinah-8.html
http://studopedia.ru/4_93117_okislitelno-vosstanovitelnie-protsessi.html




