Причины изменений содержания микроэлементов в растении винограда – Физиология минерального питания
Причины изменений содержания микроэлементов в растении винограда – Физиология минерального питания
Макро- и микроэлементы, необходимые для растений, и их физиологическая роль
Общие представления о минеральном питании.
Растения питаются простыми веществами не только из воздуха (углекислота и вода – фотосинтез), но и из почвы (ионы минеральных солей – минеральное питание). Они усваивают простые неорганические соединения из внешней природы, синтезируют из них сложные органические вещества и строят свое тело.
Органические вещества растений состоят из органогенных элементов: углерода – 45%, кислорода – 42%, водорода – 6,5% и азота – 2,5% – всего 95%. Углерод, водород, кислород усваиваются растениями в результате воздушного питания. В растениях есть также 5-10% зольных минеральных элементов – они остаются после сжигания растений.
Процесс усвоения зольных элементов и азота из почвы называется почвенным или минеральным питанием растений. Снабжение растений полным набором в оптимальном соотношении минеральных элементов имеет значение для обмена растений, нормального развития, преодоления неблагоприятных воздействий окружающей среды. В сельском хозяйстве давно научились регулировать минеральное питание растений с помощью агроприемов и внесения минеральных удобрений.
Макро- и микроэлементы, необходимые для растений, и их физиологическая роль.
Анализ обнаруживает в растениях почти все элементы периодической системы Менделеева. Главные из них – микро- и макроэлементы.

Их содержание в растениях колеблется от 0,01-10% от сырой массы растения. Необходимые макроэлементы растений: азот, фосфор, калий, кальций, магний, сера, натрий, кремний, железо, селен С помощью гравийных и водных культур была показана их необходимость для растений и были разработаны специальные смеси для водных культур.
Входит в состав белков, нуклеиновых кислот, АТФ, АДФ, коферментов, хлорофиллов, цитохромов, некоторых липидов, многих витаминов, гормонов роста растений. Азот является составной частью важнейших для жизни веществ. Он непосредственно влияет на рост растений.
Входит в состав ДНК, РНК, АТФ, коферментов, фосфолипидов, сахарофосфатов, белков, многих других промежуточных продуктов метаболизма. Фосфорсодержащие вещества занимают центральное место в конструктивном и энергетическом обмене. Важна роль фосфора в фотосинтезе и дыхании. Кроме того энергия при фотосинтетическом и окислительном фосфорилировании запасается в макроэргических фосфатных связях АТФ. Фосфор важен для цветения и плодоношения растений.
Не входит в состав органического вещества, регулирует состояние цитоплазмы клеток растений, повышая ее проницаемость и уменьшая вязкость, находится в клеточном соке, принимает активное участие в осмотических явлениях клеток, движении устьиц, усиливает биосинтез крахмала, ускоряет процессы фотосинтетического фосфорилирования, отток ассимилятов. Основная роль калия – регуляторная – принимает участие в процессах обмена веществ в растении.
Содержится во всех белках, входит в состав аминокислот (метионина, цистеина, цистина), содержится в витаминах (тиамин, биотин), липоевой кислоте, сульфолипидах, коферменте А, чесночных и горчичных маслах. Дисульфидные группы участвуют в образовании третичной структуры белков, а сульфгидрильные – в образовании ферментов с участием НАД и ФАД. Сера играет важную роль в белковом и липидном обменах, в энергетике растений, важна для поддержания структуры мембран тилакоидов хлоропластов.
Содержится в растениях в органических веществах и в ионной форме, входит в состав клеточной стенки растений, в состав хромосом, мембран, стабилизируя их структуру. В свободном виде выступает в качестве антагониста калия – повышает вязкость и снижает проницаемость цитоплазмы, нейтрализует избыток органических кислот в клетках, поддерживает жизнедеятельность меристем.
Находится в составе молекулы хлорофилла и хелатов, играет роль в стабилизации структуры рибосом, регулирует состояние цитоплазмы, повышая вязкость и понижая проницаемость цитоплазмы, является кофактором многих ферментов.
Для некоторых групп растений (галофитов) засоленных мест обитания имеет важное значение. Для большинства растений не нужен.
В больших количествах содержится в листьях некоторых древесных пород (в хвое ели), входит в состав клеточных стенок древесины, панциря диатомовых водорослей. Многие растения обходятся без него.
Их содержание в растениях достигает 0,00001-0,001% сырой массы. Являются абсолютно необходимыми для жизнедеятельности растений: медь, цинк, бор, марганец, молибден и некоторые другие. Их действие строго специфично, при исключении хотя бы одного из них из питания растений нарушаются процессы жизнедеятельности, невозможна замена одного на другой.
Содержится в количестве 0,08%. В качестве кофактора входит в состав ферментов, участвующих в синтезе хлорофилла, входит в состав оксиредуктаз, в ферментный комплекс нитрогеназы, то есть участвует в азотфиксации, содержится в молекулах цитохромов, ферредоксина, участвует в процессе переноса электронов.
Встречается в составе ферментов, участвующих в биосинтезе хлорофилла, входит в состав ферментов оксидаз, участвующих в дыхании, в состав белка пластоцианина, активирует нитроредуктазу, то есть участвует в азотном обмене. Недостаток меди вызывает задержку роста и цветения.
Играет важную роль в белковом обмене, входя в состав пептидогидролаз, принимает участие в синтезе индолилуксукной кислоты (гормон растений), влияет на синтез аминокислоты триптофана, активирует ряд ферментов гликолиза и реакции ПФП.
Имеет широкий спектр действия. Влияет на деление клеток, способствуя росту корневых и надземных частей растений, участвует в прорастании пыльцы и росте завязи, способствует оттоку углеводов из хлоропластов, повышает эластичность клеточной стенки и засухоустойчивость растений.
В качестве кофактора некоторых ферментов катализирует реакции фотосинтеза и дыхания, участвует в процессе восстановления нитратов, обмене железа, поддерживает структуру мембран тилакоидов, активирует ферменты цикла Кребса, участвует в синтезе м-РНК в ядре.
Играет важную роль в азотном обмене, участвует в процессе азотфиксации, в реакциях биосинтеза белка, аскорбиновой кислоты, способствует лучшему усвоению кальция, росту корневых систем растений. При недостатке молибдена, рост растений тормозится.
Кроме перечисленных микроэлементов важную роль играют в метаболизме растений селен, иод, ванадий, титан, никель.
77.243.189.108 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Физиология минерального питания – Роль микроэлементов в регулировании роста и плодоношения винограда
Содержание материала
М. Фрегони, А. Шиенца
РОЛЬ МИКРОЭЛЕМЕНТОВ В РЕГУЛИРОВАНИИ РОСТА И ПЛОДОНОШЕНИЯ (ПРОДУКТИВНОСТИ И КАЧЕСТВА) ВИНОГРАДНОЙ ЛОЗЫ. ПРОБЛЕМЫ ДИАГНОСТИКИ
Разграничение макро- и микроэлементов является выражением их неодинакового количественного использования в различных органах растения. Действительно, в то время как макроэлементы сильно пластичны, микроэлементы обладают способностью ускорять процессы обмена каталитически. Хотя все метаболические процессы, обусловливаемые микроэлементами, не изучены полностью ввиду их сложности, все же можно предположить, что не существует такой физиологической функции, которая могла бы обойтись без участия одного или более микроэлементов. Действие микроэлементов в основном проявляется в установлении связи металла с энзимом или же в качестве компонента самого энзима. Микроэлементы, играющие существенную роль в физиологических функциях виноградной лозы, следующие: железо, бор, марганец, цинк, медь и молибден. Кобальт, ванадий и др. также играют немалую роль, но знания о них в области виноградарства весьма скудны и отрывочны.
НОВЫЕ АСПЕКТЫ ЗНАЧЕНИЯ МИКРОЭЛЕМЕНТОВ ДЛЯ ВИНОГРАДА
Железо.
Особенно необходимо в разные фазы синтеза хлорофилла и для развития хлоропластов. Его метаболически активной формой являются гемопротеиновые энзимы (каталаза, пероксидаза, цитохромоксидаза и др.), участвующие в окислительно-восстановительных реакциях процессов фотосинтеза, дыхания, метаболизма углеводов и редукции нитратов до нитритов (Zhiznevskaya, 1972). На известняковых или бедных железом почвах наблюдаются симптомы железного хлороза, появлению которого, кстати, способствуют и другие причины, как, например, высокое значение pH, высокий процент глины и повышенное содержание фосфора (Fregoni, Scienza, 1975). Повышенное содержание марганца также оказывает антагонистическое действие при абсорбции и использовании Fe (Frеgоni, 1970). Высокий уровень меди в почве благоприятствует появлению типичных признаков железного хлороза, вызванных токсичностью меди (Fregoni, Scienza, 1974). Наоборот, наличие органического вещества и калия повышает содержание меди в листьях.
Хотя бор не входит в состав энзимов, он оказывает влияние на реакции окислительного типа (каталазу, полифенолоксидазу, пероксидазу), активизируя, таким образом, синтез хлорофилла и образование сахаров. Кроме того, бор играет роль в транспорте сахаров, так как, связываясь с ними, он легко переходит через клеточные мембраны. Он участвует в азотном метаболизме, в механизме действия гибберелинов и в синтезе бета-индолилуксусной кислоты, кроме их транспорта (Skok, Mcilroth, 1958). Он оказывает также влияние на поглощение и подвижность кальция в растении. Растения, богатые флавоноидами, испытывают наибольшую потребность в боре. Он вызывает синтез лигнина, так как принимает участие в метаболизме фенолов и фенилаланина (F1aig, 1972). Действительно, при нехватке бора наблюдается значительное накопление фенолов, не превратившихся в лигнин (Sко1niк, Мajеvsкaiа, 1970). Бор благоприятствует прорастанию пыльцы, удлинению пыльцевых трубок, т. е. процессам размножения, так как действует на синтез пектина, из которого состоит пыльцевая трубка (Vasil, 1964). Недостаток бора сказывается особенно на меристематических тканях и вызывает уменьшение синтеза РНК и ДНК, что отрицательно сказывается на явлениях дифференциации тканей и размножения клеток (Sко1niк, 1965). Сокращается также рост корней из-за деформации клеточных стенок, вызванной недостачей нуклеиновых кислот (Вuss1еr, 1960).
Марганец.
В противоположность железу и меди, марганец, так же как и бор, не участвует ни в одном известном металлическом энзиме. Все же марганец катализирует некоторые энзиматические реакции (фосфорилирование, редукцию, декарбоксилирование) и участвует в важных процессах обмена — дыхании, фотосинтезе (фотолизе воды), синтезе хлорофилла и аминокислот. Кроме того, он имеет существенное значение для конечной фазы редукции нитратов до аммиака (Ambеrgеr, 1972). Вместе с другими микроэлементами он регулирует обмен посредством индолилуксусной кислоты. Этот микроэлемент накопляется в больших количествах в растениях, богатых танином, или в органах, богатых таниновыми веществами.
Участвует во многих энзиматических системах, в частности, дыхательных, включается в обмен сахаров и протеинов, стимулирует синтез ауксина путем образования триптофана. Кроме того, так как он оказывает подавляющее влияние на полифенолоксидазу, он уменьшает окислительный распад индолилуксусной кислоты. Цинк повышает, вместе с бором и медью, засухоустойчивость, снижая испарение растений. Нехватка цинка часто наблюдается в Калифорнии и Мексике, на песчаных или обильно удобренных фосфором почвах.
Некоторые подвои и сорта винограда проявляют повышенную чувствительность к недостатку цинка.
Играет существенную роль в процессах дыхания, в частности, входит в состав аскорбиноксидазы, цитохромоксидазы и полифенолоксидазы.
Действуя на активность этих энзимов, медь катализирует синтез антоцианов. Она играет немалую роль в обмене белков и индолилуксусной кислоты. При нехватке меди, впрочем, наблюдающейся очень редко, действительно снижается активность полифенолоксидазы (F1aig, 1972), тогда как активность пероксидазы повышается (Kovalenko, 1969). Чаще имеет место интоксикация вследствие прогрессирующего обогащения медью почвы под виноградниками в результате постоянных обработок против мильдью препаратами меди (Fregoni, Scienza, 1974 а).
Молибден.
Выполняет преимущественно каталитические функции, в особенности в метаболизме азота (нитраторедуктаза). Так как существует антагонизм между молибденом и медью, молибденом и марганцем, молибденом и алюминием, токсичность марганца, меди и алюминия понижается.
Физиология минерального питания – Причины изменений содержания микроэлементов в растении винограда
Содержание материала
Кроме причин, связанных с почвенными условиями (характер материнской породы, педогенетические процессы, физические свойства почвы, pH и др.) и агротехникой (регулирование содержания извести, органическое и минеральное удобрения, обработка ядохимикатами, орошение и др.), существуют генетико-биологические и сезонные факторы, вызывающие изменения содержания микроэлементов в растении в целом и в отдельных его органах — селективность подвоев, сортовые различия и факторы окружающей среды.
Уровень микроэлементов в различных органах растения винограда
Железо.
Данные о содержании железа многочисленны, так как его частая нехватка становится причиной тяжелых проявлений хлороза. В связи с этим Sаrоsi (1964, 1975) считает, что уровень железа в листьях ниже 100 ppm; является показателем его недостатка и предлагает в качестве оптимальных величин 110—160 ppm (осенью). Christensen (1969) устанавливает, однако, в черешках листьев кустов без симптомов недостатка уровень 80 ppm при образовании завязей и 53 ppm в начале созревания. По данным L a f о η с сотр. (1964) в листьях при образовании завязей содержание железа составляет 39 ppm, в начале созревания — 170 ppm и при созревании — 203 ppm; Beyers (1962) в Южной Африке устанавливает в листьях предельные уровни 60 и 180 ppm.
В Италии Fregoni и Scienza обнаруживают в результате пятилетних исследований, что уровень железа в листьях (пластинках) варьирует от 173 до 500 ppm. При образовании завязей содержание железа обычно несколько ниже (131—436 ppm), чем в начале созревания (216—564 ppm). Rоssi (1975) определяет в области Эмилия-Романья среднее содержание железа 132—198 ppm. Значительно более низкий уровень (47—97 ppm) наблюдают Jung, Im (1972) в Корее, но наряду с очень высоким уровнем марганца, считающимся токсическим (824—2596 ppm). Кiri1уuk (1976) отмечает, что, как правило, в листьях содержится больше микроэлементов, чем в побегах, сусле и вине. В частности, он наблюдает накопление железа в листьях в ходе созревания и снижение количества бора и марганца. Содержание железа в листьях составляет примерно 302—3220 pmm.
Далее отмечается, что содержание железа повышено в листьях, находящихся у основания побегов, по сравнению с находящимися в верхней зоне и понижено в черешках по сравнению с пластинками, так как оно малоподвижно. Действительно, данные Carles с сотр. (1964) показывают, что в пластинках листьев содержится между 206 и 306 ppm железа, тогда как содержание его в черешках составляет 57—60 p pm при соотношении пластинка: черешок 3,6:5,1. В гроздях содержание железа колеблется в пределах от 45 до 58 ppm (Fregoni, Scienza, 1975а), в то время как только в ягодах оно составляет 60—78 ppm.
Молодые побеги содержат 60—70 ppm железа, тогда как вызревшие — 111—161 ppm. Содержание железа в конусе нарастания выше (103—122 ppm), чем в остальной части побега (Fregoni, Scienza, 1976). Корни довольно богаты железом — от 194 до 199 ppm (Fregoni, Scienza, 1974а) в противоположность семенам, оказавшимся наиболее бедными этим элементом— 43—47 ppm (Fregoni, Scienza, 1976 а). В соке Dogramadjian (1975) установил уровень железа 2—5 ppm.
Тесно связан с содержанием железа уровень марганца, так как эти два элемента находятся в антагонистических отношениях.
Этот антагонизм выражается в значениях соотношения железо: марганец. В кустах, выращенных на питательном растворе, это соотношение колеблется от 0,99 до 0,48 в зависимости от наличия или отсутствия железа в среде. Считается, что железный хлороз проявляется при значениях этого соотношения ниже 1. Delmas (1975) считает оптимальным для гидропонной культуры винограда соотношение 1 во время цветения и 0,6 в начале созревания. Когда это соотношение превысит 5, возникает нехватка марганца. В итоге пятилетних исследований Fregoni и Scienfa в Италии установили нормальное значение соотношения железо: марганец в листьях 2,25:2,46 (табл. 2). Dogramadjian (1975) считает, что соотношение железа и марганца в пасоке имеет значительную диагностическую ценность в отношении установления морозостойкости некоторых сортов. Действительно, у морозостойких сортов это соотношение составляет 0,15, тогда как у неморозостойких оно колеблется в пределах 0,1—0,6.
Таблица 2
Содержание микроэлементов (ррт) в листьях при образовании завязей (А) и и начале созревания (I) на нескольких виноградниках Италии, определенное техникой листовой диагностики (1974—1976) 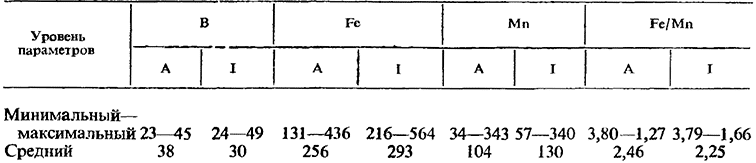
Sаrоsi (1975) считает оптимальным содержание бора 30—50 ppm в 8-м листе осенью. Christensen (1969) при помощи техники листовой диагностики определяет в черешках листьев 40 ррm при образовании завязей и в начале созревания. Аналогично этому Sarosi на основании имеющейся в их распоряжении обширной информации считает нормальным для условий Италии содержание бора в листьях от 25 до 41 ppm (23—47 ppm при образовании завязей и 24—49 ppm в начале созревания) (табл. 2). Levy (1968) считает, что 25—40 ppm — нормальное содержание. Gartel (1956, 1974) считает оптимальным содержанием бора в листьях 15—38 ppm, в то время как недостаток его проявляется на уровне ниже 9—10 ppm. Кiri1уuк (1976) устанавливает в листьях в зависимости от сорта значительно более высокое содержание — 141—298 ppm. По мнению Lafоn с сотр. (1964) нормальный уровень бора в листьях колеблется от 20 до 23 ppm соответственно при образовании завязей и в начале созревания, в то время как в побегах в это же время он составляет 20—14 ppm, а в гроздях — 25—28 ppm. Fregoni и Sciеnzа (1974а) устанавливают уровень бора в побегах 31—44 ppm, в вызревших побегах — 42—57 ppm и в корнях — 48—68 ppm. Особенно высоким является содержание этого элемента в семенах — 75—85 ppm (Fregoni, Sсiеnzа, 1976a).
Cartel (1974) утверждает, что определение содержания бора в сусле является отличным способом установления потребности виноградной лозы в подкормке бором. Оно должно составлять 2—5 ppm в нормальных случаях, недостаток же наступает при уровне ниже 1—1,5 ppm.
Значение бора для оплодотворения подтверждается высоким уровнем этого микроэлемента в органах цветка. Gаrtе1 (1962а) устанавливает в рыльце 50—60 ppm, в то время как в секрете рыльца в ранние утренние часы содержится 2—5 ppm (40—140 ppm в сухом веществе). При падении уровня бора до 8—10 ppm оплодотворение понижается. В пасоке по Dogramadjian (1975) содержится в зависимости от сорта 0,032—0,75 ppm бора.
Большое значение имеет токсичность в результате чрезмерного внесения борных удобрений. Вредным считается содержание бора в пластинках листьев в количестве 700—1000 ppm и в черенках — 100—300 ppm (Gаrtе1, 1974). Levy, и Chaler (1964) считают все же, что уже уровень бора в листьях выше 60 ppm является токсичным. Beyers (1962) считает нормальным уровень бора в листьях 25—100 ppm и токсичным — выше 400 ppm.
Марганец.
Явления недостаточности этого элемента не имеют существенного значения, более важные проявления его токсичности в почвах с низкими значениями pH и богатых марганцовыми солями. Badour и Levy (1964) считают нормальным содержание марганца в листьях 30—80 ppm, тогда как недостаток отмечается на уровне 5—25 ppm. Sаrоsi (1975) считает оптимальным содержание марганца в листьях осенью 57—130 ppm. Christensen (1969) устанавливает в черешках листьев со стороны, супротивной грозди, уровень марганца 56 ppm при образовании завязей и 54 ppm — в начале созревания. Нормальное содержание марганца в листьях в области Эмилия составляет 80—112 ppm (Rоssi, 1975). Beyer (1962) определяет в Южной Африке от 20 до 300 ppm марганца в листьях. Токсичный уровень — 1000 ppm.
Листья являются наиболее богатыми марганцем органами растения винограда (2/5 всего количества этого элемента содержатся в листьях). Нормальный уровень, по мнению Gartel, составляет 30—60 ppm. Исследованиями Fregoni и Scienza установлено, что содержание марганца в листьях винограда в условиях Италии колеблется примерно от 104 ppm при образовании завязей до 130 ppm в начале созревания с максимумом 600 ppm (табл. 2). Несмотря на столь высокий уровень, он никогда не вызывал явных симптомов токсичности, быть может потому, что сопровождался столь же высоким содержанием железа. Кiri1уuк (1976) установил в листьях сортов Рислинг и Каберне Совиньон содержание марганца 114—190 ppm. Carles с сотр. (1964) установили, что содержание марганца в пластинках листьев выше (40—70 ppm), чем в черешках (16—32 ppm), при соотношении пластинка: черешок 2,2 :2,5. Это позволяет утверждать, что черешок контролирует переход марганца в пластинку листа. К полностью противоположным выводам пришел Sаrоsi (1975), считающий повышенное содержание марганца в черешках листьев показателем его значительной подвижности в растении. Бедны марганцем древесина вызревших побегов (10—15 ppm) и семена (7—10 ppm), тогда как в сусле его содержание 0,4—1,4 mg/1 (Sabatelli с сотр., 1972; Gartel, 1974). В вине Чинкуе терре содержится до 3,4 ppm. Lafоn с сотр. (1964) установили в листьях 17—19 ppm соответственно при образовании завязей и в начале созревания, 6—7 ppm в молодых побегах и 5—15 ppm в гроздях. На повышенные значения указывают аналитические результаты Frеgonin Scienza (1974а, 1976): в ягодах — около 5—6 ppm, в конусе нарастания — 17—24 ppm, в семенах — 10—12 ppm, в побегах — 27—32 ppm и в корнях — 26—31 ppm. Sabatelli с сотр. (1972) установили для сорта Кьянти величины в среднем 19 ppm в гребнях гроздей, 6 ppm — в кожице ягод, 0,4 ppm — в мякоти и 19 ppm — в семенах.
Различия нередко объясняются принятыми аналитическими методами. По мнению Ribereau-Gayon и Peynaud (1960) существует избирательная концентрация в различных частях ягоды в соотношении семена: кожица:мякоть — 30:10:1. По данным Dogramadjian (1975) в пасоке содержится в среднем 0,32—1,87 ppm. Что же касается токсичности, Vidal с сотр. (1969) установили симптомы заболевания при содержании марганца в листьях от 221 до 3000 ppm. Gаrtе1 (1974) считает токсическим уровень марганца в листьях от 1200—1800 ppm до 5000 ppm. Такой уровень считают токсическим также Badour и Levy (1964). Вranas (1974) установил проявления токсичности при уровне марганца в листьях 45—230 ppm в зависимости от расположения побега.
Цинковая недостаточность винограда в Европе — явление редкое и возникает лишь в случаях внесения высоких доз фосфора (Gаrtе1, 1974). Уровень 25—60 ppm в листьях считается нормальным, 2—16 ppm — недостаточным (Gаrtе1, 1974). Christensen и Kasimatis (1967) установили в черешках листьев содержание цинка 10—17 ppm в мае и 22—27 ppm в июле. Christensen (1969) считает нормальным уровнем цинка в черешках 30 ppm при образовании завязей и 34 ppm в начале созревания. Sаrоsi (1975) считает содержание 20—22 ppm в восьмом листе достаточным, уровень 15 ppm уже указывает на латентную недостаточность. Frеgоni и Sсiеnzа (1974а) установили в здоровых кустах с интоксикацией медью уровень цинка в листьях 87—120 ppm, в побегах — 48—51 ppm, в вызревших побегах — 39—71 ppm и в корнях — 38—59 ppm. По данным Gаrtе1 (1974) наиболее высоко содержание цинка в меристематических тканях; богаче всего листья (в них содержится около 30—40% всего количества цинка в растении), молодые побеги и почки. Древесина побегов наиболее бедна цинком. В сусле содержится около 3—5 ppm (Gаrtе1, 1955).
Недостатка меди практически не бывает, однако считается, что ее нормальный уровень в листьях колеблется от 4-8 (Sаrоsi, 1975) до 40— 50 ppm (Carles с сотр., 1966). Значительно большее содержание меди установлено в листьях—185—424 ppm (Кri1уuк, 1976). Одревесневшие побеги и ягоды — самые бедные медью части лозы. Молодые побеги содержат 17— 26 ppm меди, а грозди и побеги — 21—27 ppm (Саr1еs с сотр., 1966; Frеni, Scienza, 1974). Нередко обнаруживается интоксикация в результате накопления меди в почве, причем наиболее чувствительны корни. Gаrtеl (1974) установил уровень меди 178 ppm в корнях в почве, обогащенной медью, против 6 ppm в корнях в нормальной почве. Fregoni и Scienzа (1974) в условиях интоксикации медью установили в корнях растений содержание меди 100 ppm, тогда как в корнях нормальных кустов ее содержание не превышало 48 ppm. В сусле содержалось около 0,2—4 mg/l меди. Если, однако, кусты обрабатывались содержащими медь препаратами, ее содержание в сусле возрастало до 6—25 mg/l (Gаrtе1, 1974).
Ценным диагностическим методом, кроме анализа корней, оказалось определение активности пероксидазы и полифенолоксидазы в вытяжках листьев. При наличии симптомов токсичности активность этих энзимов понижается до 50% и возрастает в 6 раз. Изменяется также содержание хлорофилла — общего, „а“ и „б“, но в первую очередь варьирует соответственное соотношение (Fregoni, Scienza, 1974).
Молибден.
Симптомы недостаточности этого элемента установлены только у растений, выращивавшихся на питательных растворах, и никогда — на виноградниках, Из проведенных Gаrtе1 исследований (1974) явствует, что наиболее богата молибденом пыльца (около 1 ppm), тогда как в листьях его содержится около 0,2 ppm.
Древесина наиболее бедна молибденом — 0,1 ppm. Сусло содержит от 0,0047 до 0,169 mg/l молибдена, вино — от 0,0011 до 112 mg/l. Delmas (1975) установил, что недостаток молибдена вызывает обогащение листьев марганцем и кальцием и обеднение калием.
Сезонные колебания основных микроэлементов в различных органах растения винограда
Железо.
В листьях молодых побегов и в ходе вегетации динамика содержания этого элемента неравномерна. Наиболее высок его уровень в начале созревания в черешках листьев, находящихся у основания побега (Christensen, 1969; Sаrоsi, 1975). Fregoni и Scienza установили, что в ягодах оно возрастает до начала созревания и затем по мере созревания прогрессивно снижается (рис. 2). Аналогичное развитие наблюдается при выражении содержания железа в mg/l000 ягод; т. е. кривая роста имеет форму двойного сигмоида. Lafon с сотр. (1964) констатировали, что ритм поглощения этого элемента достигает максимума в листьях и молодых побегах в фазе после начала созревания, тогда как в гроздях непрерывно возрастает до сбора урожая.
Величина этого микроэлемента в черешках листьев на протяжении побега и во время вегетации довольно постоянна (Christensen, 1969). Исследования Lafon с сотр. (1964) показывают, что поглощение бора молодыми побегами и листьями возрастает до начала созревания, затем понижается. В гроздях содержание бора такое же, как и железа. Fregoni и Scienza отмечают максимальное содержание этого элемента в ягодах в начале созревания (рис. 2). В пересчете на сухое вещество на 1000 ягод содержание бора возрастает до начала созревания и задерживается на постоянном уровне до сбора урожая.
Марганец.
Содержание марганца в черешках листьев возрастает по мере созревания, независимо от расположения листьев на побеге (Christensen, 1969). Что же касается ритма поглощения, наблюдается постоянный рост (в листьях, побегах и гроздях) до созревания (Lafon с сотр., 1964). В ягодах содержание марганца достигает максимального уровня к началу созревания (в ppm или в сухом веществе на 1000 ягод) (Fregoni, Scienza) (рис. 3).
Источники:
http://studopedia.ru/11_45774_makro–i-mikroelementi-neobhodimie-dlya-rasteniy-i-ih-fiziologicheskaya-rol.html
http://vinograd.info/knigi/fiziologiya-vinograda-stoev/fiziologiya-mineralnogo-pitaniya-13.html
http://vinograd.info/knigi/fiziologiya-vinograda-stoev/fiziologiya-mineralnogo-pitaniya-15.html




