Количественное цитохимическое определение крахмала в тканях виноградного растения
Количественное цитохимическое определение крахмала в тканях виноградного растения
Количественное цитохимическое определение крахмала
Определение крахмала в растительном материале обычными методами биохимического анализа, несмотря на их формальную точность, не всегда дает достаточно удовлетворительные результаты. Во многих случаях более точными в биологическом смысле являются показатели содержания крахмала, полученные путем цитохимического определения на срезах тканей под микроскопом. В основе определения лежат общие принципы микрохимии растений (Л.И.Джапаридзе, 1953)
Определения можно проводить как на свежем, так и на консервированном материале. Однако способ хранения и обработки материала должен быть одинаковым для всех сравниваемых образцов, так как он может оказать влияние на состояние крахмальных зерен и восприимчивость их к реактивам. Для консервирования образцов древесины виноградного растения удовлетворительной средой является смесь равных частей этилового спирта, глицерина и воды с прибавлением одного процента формалина. Входящий в состав смеси глицерин способствует некоторому размягчению одревесневшего материала и облегчает его резку.
Срезы, выполняемые на микротоме или от руки, должны иметь строго определенную толщину, поскольку с ее изменением при одном и том же содержание крахмала в клетках изменяются оптическая плотность и насыщенность окраски препарата.
Цитохимическое определение крахмала в материале, не залитом в парафин или иную среду, необходимо вести на срезах, включающих один слой (ярус) неповрежденных клеток. В противном случае крахмал в процессе резки и обработки препаратов теряется и данные учета оказываются заниженными.
При просмотре очень толстых срезов, включающих несколько слоев клеток, степень заполнения их крахмалом будет казаться большей, чем она есть в действительности ( вследствие оптического наложения друг на друга клеток, находящихся на разных уровнях ).
На поперечных срезах крахмал особенно легко теряется при повреждении клеток лучевой паренхимы. Если учесть, что поперечник их в древесине различных органов винограда равен 20-25 мк, то для цитохимического исследования следует брать срезы толщиной около 30 мк. При изучении осевых органов в большинстве случаев можно ограничиться определениями на поперечных срезах, однако для контроля следует использовать также продольные тангентальные срезы толщиной около 30 мк.
В качестве реактива при цитохимическом определении крахмала применяют 0,2-пропентный раствор йода с йодистым калием, для приготовления которого 1 г К йод растворяют при нагревании в 5 мл дистиллированной воды, после чего в этот же раствор добавляют 1 г кристаллического йода. Полученный раствор разбавляют до 500 мл и хранят в темноте в склянке с хорошо притертой пробкой. При обработке различных препаратов следует пользоваться раствором одинаковой концентрации. Порча раствора, связанная с выделением йода, требует его периодической замены свежеприготовленным раствором.
Срезы споласкивают в дистиллированной воде, помещают на 1 минуту в 1-процентный раствор НСl ,затем переносят мягкой кистью на часовые стекла или в неглубокие стаканчики и. покрывают пятью-шестью каплями раствора. Для массовой работы весьма удобны многогнездовые кюветы, которые можно изготовить из чашек Петри. Срезы выдерживают в растворе 10-15 минут, наблюдая за тем, чтобы они были полностью покрыты жидкостью. Через некоторое время крахмальные зерна приобретают фиолетовую окраску раз – личной интенсивности. После этого срезы переносят на предметное стекло в каплю глицерина, покрывают покровным, стеклом и исследуют под микроскопом. Исследование проводят при верхнем положении конденсора микроскопа и достаточно высокой интенсивности освещения. Слабое и переменной силы освещение приводит к ошибкам в определении. Поэтому необходимо пользоваться осветителем ОИ-7 (с синим светофильтром) или осветителями, входящими в комплект биологических микроскопов.
Для цитохимического определения крахмала в тканях органов винограда можно пользоваться микроскопом с увеличениями от 7×8 до 7×40.
Принцип количественного учета при цитохимическом определении крахмала основан на глазомерной оценке степени заполнения крахмалом полостей клеток по десятибалльной шкале и подсчете числа клеток, содержащих крахмал, по отношению к общему числу их в поле зрения микроскопа. Суммарный итог выражают в процентах. Приводим конкретный пример соответствующего расчета. В поле зрения микроскопа на срезе виноградного побега 25 клеток лучевой паренхимы. Пять из них не содержат крахмала, у двух клеток крахмальные зерна заполняют 2/10 клеточной полости, у десяти – 5/10 и у восьми – 8/10. Суммарное заполнение полостей клеток крахмалом составляет: 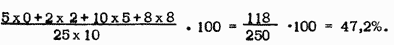
Учет содержания крахмала следует проводить раздельно для разных тканей или структурных элементов исследуемого органа.
Осевые органы виноградного растения включают следующие крахмалсодержащие ткани и структурные элементы: в древесине – лучевая паренхима, либриформ, древесная паренхима, обкладочные клетки, перимедуллярная зона; в коре – лубяная паренхима, твердый луб, феллодерма, а также клетки, примыкающие к перицикловым волокнам (в первичной коре). Доля каждого из этих элементов по отношению к общему объему тканей зависит от принадлежности их к тому или иному органу, от его состояния, собственного и общего возраста органов и т.д.
Относительный объем отдельных структурных элементов, способных к накоплению крахмала, может быть найден путем микрометрических измерений на анатомических срезах органа. На основе такого определения ‘с учетом фактического содержания крахмала могут быть получены средневзвешенные показатели количества его в клетках органов и частей виноградного растения.
Важными показателями, характеризующими биохимические свойства крахмала, являются диаметр его зерен, интенсивность окраски и быстрота потери ее после окончания воздействия красителя. Эти свойства необходимо по возможности учитывать в ходе цитохимических определений крахмала.
В наших исследованиях количественное цитохимическое определение крахмала в многолетних частях виноградных кустов позволило выявить картину его локализации по тканям разного возраста, динамику его изменений на протяжении годичного цикла развития растений и влияние старения тканей на интенсивность крахмального обмена.
При тщательном проведении работы количественное патохимическое определение крахмала позволяет получить данные, мало отличающиеся от показателей, харастеризующих динамику абсолютного количества крахмала, приходящегося на одну клетку виноградного побега (рис. ).

Динамика содержания крахмала в побегах винограда: 1 – в процентах к сухому веществу; 2 – вес, приходящийся на одну клетку; 3 – процент заполнения полостей клеток по данным цитохимического определения.
Количественное определение крахмала в тростниковом сахаре-сырце Текст научной статьи по специальности «Промышленные биотехнологии»
Похожие темы научных работ по промышленным биотехнологиям , автор научной работы — Чугунов А. И., Егорова М. И., Беляева Л. Й., Чугунова Л. С., Милых А. А.
Текст научной работы на тему «Количественное определение крахмала в тростниковом сахаре-сырце»
кислот. Однако следует отметить, что в условиях относительно небольшого содержания спирта (не выше 60%) даже при достаточном подкислении испытуемого раствора выход основной реакции, по-видимому, небольшой и отсюда получаются заниженные результаты по пероксидному числу.
Поэтому все операции пробоподготовки косвенного потенциометрического метода определения содержания гидроперикисей в эфирных маслах проводили в соответствии со стандартной методикой [3] (растворение пробы масла в ледяной уксусной кислоте, ее нейтрализация бикарбонатом натрия и введение дозы насыщенного раствора йодида калия). Но вместо титрования рабочим раствором тиосульфата натрия измеряли равновесное значение потенциала «точечного» платинового электрода ¿Гь вносили 0,5 -1,0 см3 фикса-нального раствора йода – с (1/2 12) = 0,1 моль/дм3 – и измеряли значения потенциала^. Массовую долю пероксидов X, %, в пересчете на активный кислород вычислили по формуле
где 5 – крутизна электродной функции, экспериментальное значение которой (24,5 мВ) было найдено из градуировочной характеристики Е – с (12) в данных экспериментальных условиях.
Получены следующие результаты параллельных определений пероксидного числа, % активного кислорода: шалфей – 0,144; 0,157; 0,148; 0,144; 0,156; 0,147; 0,144; 0,137; 0,125; 0,111; 0,127; 0,147; кориандр -0,207; 0,228; 0,240; 0,241; 0,208; 0,188; 0,202; 0,229.
Найдено х, мг КОН/г
Масло Титриметрия х по [3] Потенциометрия х ± Дх п Sr- 10’2
Кориандровое 0,23 0,218 ±0,016 8 8,4
Шалфейное 0,14 0,14 ± 0,09 12 9,6
Результаты определения имеют удовлетворительные метрологические характеристики (таблица), в том числе в сравнении с отраслевыми нормативами [3-4].
Разработан нетитриметрический потенциометрический йодометрический метод определения органических пероксидов (пероксидного числа) в эфирных маслах с удовлетворительными метрологическими характеристиками.
1. Выскубова Е.Н., Цимбаленко Е.А., Морозова О.В., Шару-дина С.Я. Редокс-потенциометрический нетитрометрический метод определения пероксидного числа эфирных масел // Совр. проблемы теорет. и эксперимент, химии: Тез. докл. II Всерос. конф. молодых ученых. – Саратов: Изд-во Саратов, ун-та, 1999. – С. 114.
2. Турьян Я. И. Зависимость констант нестойкости комплексных ионов от диэлектрической постоянной растворителя // Журн. неорган. химии. – 1959. – 4. -№ 4. – С. 813-817.
3. ГОСТ 14618.3-78. Масла эфирные, вещества душистые и полупродукты их синтеза. Методы определения перекисей. – М.: Изд-во стандартов, 1986. – С. 31-35.
4. ГОСТ 28687-90 (СТ СЭВ 6763-89) Реактивы. Методы определения пероксидов в органических растворителях. – М.: Изд-во стандартов, 1990. -4 с.
Кафедра стандартизации, сертификации и аналитического контроля
Поступила 19.06.03 г
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КРАХМАЛА В ТРОСТНИКОВОМ САХАРЕ-СЫРЦЕ
А.И. ЧУГУЙОВ, М.И. ЕГОРОВА, Л.И. БЕЛЯЕВА,
Л.С. ЧУГУЙОВА, А.А. МИЛЫХ
Российский научно-исследовательский институт сахарной промышленности
Одной из основных характеристик качества тростникового сахара-сырца как объекта промышленной переработки является фильтрационная способность его растворов. Этот показатель характеризует наличие в сахаре-сырце крахмала, декстрана, других высокомолекулярных соединений, а также отдельных зольных элементов; но наибольшее влияние на фильтрационные свойства растворов оказывает крахмал (продукты его деструкции). Присутствие крахмала в сахаре-сырце связано с особенностями сырья – сахарного тростника, являющегося растением семейства злаковых.
Повышенное содержание крахмала в тростниковом сахаре-сырце вызывает серьезные затруднения при ведении технологических процессов переработки: замедляется фильтрование клеровки сахара-сырца, ухудшаются условия кристаллизации сахарозы и центрифугирования утфелей, снижается производительность завода. Крахмал, плохо удаляясь в процессе известково-углекислотной очистки, попадает в са-хар-песок и снижает его потребительские качества.
Учитывая, что сахарные заводы России ежегодно перерабатывают около 5 млн т тростникового сахара-сырца, для правильной организации технологического процесса его переработки необходимо осуществлять оперативный контроль на личия крахмала в поступающем сырье. Массовость определений предъявляет к методике соответствующие требования: простота исполнения, малая трудоемкость и длитель-
[ метод »блемы )лодых
риве-*: за-ырца, тен-ггель-цессе в са-ва.
ность при достаточной точности, возможность выполнения без использования высокоточных и редких приборов и реактивов.
Предлагаемые методы определения крахмала в сахарсодержащих продуктах основаны, как правило, на чувствительной цветной реакции крахмала с йодом. Они различаются между собой по операциям подготовки, проведения и регистрации цветной реакции. Часть методов предусматривает предварительное выделение крахмала путем его осаждения этанолом, промывки и последующего растворения, что делает их сложными, с риском потери части определяемого вещества [1-3].
Этих недостатков лишены методы, в которых цветная реакция проводится непосредственно в сахарсодержащих растворах без предварительного выделения крахмала [3-5]. Поэтому в качестве основы оперативного контроля нами был экспертно отобран упрощенный метод определения крахмала [4].
Инструментальная проверка метода выявила, что при определении крахмала непосредственно в сахарсодержащих растворах не исключается влияние на цветную реакцию посторонних веществ, что может привести к систематической ошибке. Кроме того, в данном методе не учитывается цветность самих анализируемых растворов, а раствором сравнения как при построении калибровочной кривой, так и при определении оптической плотности окрашенного комплекса служит раствор, учитывающий лишь цветность применяемых реактивов. Эго ведет к систематическому завышению результатов определения оптической плотности окрашенного комплекса в анализируемых пробах сахара-сырца. В связи с этим нами было введено понятие «нулевой пробы», под которой подразумевается оптическая плотность сахарного раствора, обусловленная присущими ему красящими веществами. По нашим данным, величина ошибки определения без учета этой цветности может достигать 80% (табл. 1).
Поэтому при проведении анализов этим методом было предложено ввести поправку на оптическую плотность «нулевой пробы», которую следует вычитать из оптической плотности анализируемых растворов после проведения цветной реакции.
Говоря о крахмале тростникового сахара-сырца, имеют в виду и продукты его превращения, образовавшиеся в условиях высоких температур и щелочной среды, т. е. это клейстеризованный и частично гидролизованный крахмал. Поэтому при построении калибровочной кривой целесообразно использовать не нативный картофельный крахмал, а растворимый, который частично гидролизован и, следовательно, ближе по составу к крахмалу’ тростникового сахара-сырца [6].
На рис. 1 изображена зависимость оптической плотности водного раствора от содержания крахмала в нем. Данная зависимость от начала координат до концентраций крахмала 0,5-0,6 мг/см3 прямолинейна, при
Место отбора пробы сахара-сырца
исследуемого раствора Д нулевого раствора До окрашенного комплекса Д
ОАО «Сахарный комбинат Льговский» 0,480 0,194 0,286 68
АО «Лопандино-сахар» 0,516 0,240 0,276 67
ОАО «Сахзавод Олымский» 0,842 0,240 0,602 30
ООО «Пром-сахар» 0,495 0,160 0,335 48
ОАО «Колпнян-ский сахзавод» 0,618 0,280 0,338 83
АО «Товарково-сахар» 0,622 0,134 0,488 27
больших же концентрациях крахмала кривая носит выпуклый характер и отступает от закона Бера.
Чтобы проверить влияние сахарозы на цветную реакцию, были получены кривые зависимости оптической плотности от содержания крахмала в 1 см3 водных и сахарсодержащих растворов различной концентрации (рис. 2: 1- вода; 2 – раствор свекловичного сахара; растворы тростникового сахара-сырца: 3, 4 -ОАО «Сахарный комбинат Льговский», 5,6- ОАО «Сахзавод Олымский» с концентрацией 36% (3,5) и 55% (4,6)).
Графики показывают, что во всех случаях наблюдается прямолинейная зависимость, т. е. соблюдается закон Бера. Линии для растворов свекловичного сахара-песка и воды исходят из начала координат и практически совпадают, что указывает на отсутствие крахмала в сахаре-песке и влияния сахарозы на цветную реакцию крахмала с йодом.
Линии для растворов тростникового сахара-сырца также имеют прямолинейную форму, однако берут начало на оси ординат, образуя на ней отрезок тем больший, чем выше концентрация сахара, что свидетельствует о присутствии крахмала в сахаре-сырце. Угол наклона кривых в большинстве случаев не отличался от угла наклона линий для воды и сахара-песка, что указывает на отсутствие в саха-ре-сырце несахаров, влияющих на цветную реакцию. Отклонение линии 6 для раствора с концентрацией сахарозы 55%, наблюдающееся при оптической плотности 1,5-1,6, скорее всего объясняется более высоким содержанием крахмала, что позволило достигнуть области, где нарушается закон Бера (рис. 1), так как для более низкой концентрации растворов того же саха-ра-сырца (36%) изменения угла наклона линии не наблюдалось.
Полученные данные позволили предложить методику количественного определения крахмала в тростниковом сахаре-сырце, в которой исключено влияние на результаты определений присутствующих в растворе сахара-сырца других окрашенных соединений пу-
Содержание крахмала, мгЛ)»!3 Расхождение результатов
введенного в сахарный раствор определенного ;:по предлагаемой методике мг/см3 % к введенному
ол . 0,331 +0,001 1,0
0,2 0.420 . +0,012 6,0
0,3 0,515 +0,017 5,6
0,4 0,618 +0,014 3,5
0,5 0,698 +0,034 6,8
0,6 0,843 +0,014 1,7
ние было незначимым для наших измерений и им можно пренебречь [7, 8].
Для нахождения величины случайной составляющей погрешности метода определяли содержание крахмала в образцах тростникового сахара-сырца с различных сахарных заводов. В табл. 3 представлены результаты одной из серий опытов, определения делались в пяти повторениях.
Как видно, величина абсолютной случайной ошибки не превышала 14 мг/кг, а относительной ошибки -6,1%, при этом точность метода оценки составила 0-20 мг/кг (при диапазоне измерений 0,1-1 г/кг сахара-сырца), т. е. данная методика может быть использована для определения крахмала в сахарсодержащих растворах в условиях заводских лабораторий.
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35 Содержание
тем введения поправки на «нулевой раствор», последняя вычитается из результата основного определения.
Для проверки предлагаемой методики в растворы тростникового сахара-сырца одного качества (СВ 35%) вводили добавки крахмала, которые затем опре-дгляли по калибровочной кривой, изображенной на рис. 1.
Полученные результаты (табл. 2) показывают, что количество крахмала, определенного в растворах сахара-сырца, оказалось большим, чем было введено, на величину (0,232 мг/см3), равную содержанию крахма-‘ ла в исходном растворе сахара-сырца. Данное значение учитывали при вычислении расхождения между введенным количеством крахмала и определенным по предлагаемой методике; как оказалось, это расхожде-
Место отбора пробы сахара-сырца Содержание крахмала, мг/кг Среднее арифметическое и его доверительный интервал, мг/кг Относительная ошибка, %
комбинат 213; 240; 214;
Льговский» 246; 230 228± 14 6,1
АО «Лопандино- 255; 252; 252;
сахар» 246; 248 251 + 4 1,1
ОАО «Сахзавод 466; 478; 482;
Олымский» 472; 486 477 ±13 2,7
ООО «Пром- 464; 471; 479;
сахар» 482; 468 472 ± 12 2,5
В результате анализа более 40 образцов из различных партий сахара-сырца, поступившего для переработки на сахарные заводы в 2001-2002 гг., установлено, что наименьшее количество крахмала находилось в сахаре-сырце из Никарагуа, Сальвадора и Гватемалы – (100-190 мг/кг), наибольшее – из Кубы и Колумбии – до 490 и 560 от/кг соответственно. Наиболее высокое содержание крахмала установлено в партии сахара-сырца, поступившего для переработки на ООО «Сахарный комбинат Большевик» в 2002 г. из Таиланда; в отдельных пробах оно колебалось от 700 до 2500 мг/кг, что вызвало затруднение при проведении технологических процессов.
Таким образом, как показала апробация, указанная методика удовлетворяет требованиям, необходимым для массовых определений в условиях заводских лабо-
Справочник химика 21
Химия и химическая технология
Определение крахмала
Раствор иода окрашивает крахмал в синий цвет. Эта реакция широко используется в анализе для определения крахмала или иода. [c.359]
Расхождение между параллельными определениями крахмала прн длине трубки сахариметра 2 дм допускается ие более 0,5%, при длине 1 дм — не более 1,0%. [c.273]
Существенный недостаток определения количества крахмала методом кислотного гидролиза заключается в том, что наряду с крахмалом частично расщепляются и гемицеллюлозы, вследствие чего искажаются данные об истинном содержании крахмала. Особенно это наблюдается при анализе растительных продуктов, содержащих много гемицеллюлоз. Чтобы избежать этого, был разработан диастатический (ферментативный) метод определения крахмала. Обработка навески растительного материала в определенных условиях диастазом позволяет отделить крахмал от других углеводов. Диастаз, как и другие ферменты, обладает строгой специфичностью и расщепляет только крахмал, переводя его в растворимое состояние. Растворимые продукты ферментативного расщепления крахмала отфильтровывают, отбирают определенное количество прозрачного фильтрата и проводят гидролиз НС1. В гидролизате определяют глюкозу описанными методами. Весьма существенным недостатком ферментативного метода является длительность определения. [c.165]
Количество образовавшейся окиси меди (I) не прямо пропорционально количеству определяемого сахара. Инвертный сахар, образующийся при определении сахарозы, требует на свое окисление несколько иного количества меди (И), чем декстроза, образующаяся при определении крахмала. Поэтому полученные результаты могут отклоняться от действительных значений до 2%. [c.375]
Определение крахмала и других полисахаридов [285, 286]. [c.294]
Для определения крахмала, например в бумаге, отбирают пробу, содержащую 0,01—0,4 г крахмала, измельчают и растирают ее с 20 мл воды. Добавляют 600 мл воды, нагретой до 50 °С, полученную жидкость нагревают до 95 °С и после охлаждения разбавляют водой до объема 1 л. Часть жидкости центрифугируют, отбирают 10 мл и добавляют 10 мл раствора 1%-ного по иоду и [c.294]
Варианты определения крахмала по реакции с иодом приведены также в работах [287—290]. [c.295]
Герасимов Б. А. Определение крахмала в зерновых объектах. Тр. Груз. с.-х. ин-та, [c.267]
Усвояемые полисахариды. Крахмал. Основным усвояемым полисахаридом пищевых продуктов является крахмал. Стандартного метода определения крахмала нет. Многочисленные методы плохо воспроизводимы, что зависит от условий их проведения [12, 20]. К тому же методы определения обусловливаются содержанием крахмала в продукте. Однако все методы предусматривают следующие стадии. [c.219]
Метод определения крахмала так называемым кислотным гидролизом, основанный на том, что растительный материал, содержащий много крахмала, кипятят с [c.81]
Остаток материала после определения крахмала переносят с воронки в прежнюю колбу, воронку смывают определенным объемом воды (50—100 мл) и для определения углеводов IV группы (гемицеллюлозы) к содержимому колбы добавляют такой объем 20%-ной НС1, чтобы во всем объеме концентрация НС1 равнялась 2%. Гемицеллюлозы гидролизуют нагреванием на кипящей водяной бане в течение 3 часов. [c.93]
По мнению Л. А. Иванова, углеводный комплекс ячменя нельзя считать хорошо изученным, так как в него входит 10— 15% гемицеллюлоз, 9—12% пентозанов, камеди и гумми, дающих при гидролизе несбраживаемые сахара и влияющих на определение крахмала. [c.20]
Потери сбраживаемых веществ. Потери сбраживаемых веществ складываются из потерь крахмала и сахаров на дыхание и крахмала на процессы синтеза новых веществ в вегетативных частях растения. Траты на дыхание совпадают с потерями сухих веществ и могут быть определены взвешиванием зерна до и после проращивания, а также определением его влажности. Потери крахмала на образование новых частей растения могут быть установлены только непосредственным определением крахмала до и после проращивания. Определения потерь при солодоращении производились неоднократно. В качестве примера в табл. 11 приведены подробные данные определения потерь сбраживаемых веществ для ячменного и просяного солода. [c.107]
ТАБЛИЦА 36 Определение крахмала в картофеле по плотности клубней [c.511]
Так же как и в химии, для определения крахмала, пользуются йодом, в присутствии которого крахмал синеет, так и для определения многих веществ, не обладающих собственным свечением, пользуются в люминесцентных методах анализа специальными реактивами, при взаимодействии с которыми образуются светящиеся составы. Таким путем, например, легко обнаруживается витамин В, приобретающий характерное свечение при взаимодействии с красной кровяной солью. [c.108]
Расчет результатов определения крахмала ведется по формуле [c.248]
Охладив содержимое колбы, в нее приливают 30 мл дистиллированной воды, и 5 мл 10%-ного раствора фосфорновольфрамовой кислоты для осаждения белков, мешающих определению крахмала. После этого объем жидкости в колбе доводят до метки дистиллированной водой и, дав отстояться, фильтруют через сухой фильтр в сухую колбу. Бесцветный фильтрат анализируют в поляриметре (см. стр. 79—81). [c.218]
Крахмал извлекался из клубней растений горячим концентрированным раствором СаСЬ определение крахмала производилось колориметрически (с йодом). [c.128]
Специфической реакцией является взаимодействие с иодом. Прп этом крахмал образует соединение, имеющее темно-синюю окраску. Эта реакция служит для качественного определения крахмала и пода. [c.430]
Предложен метод определения крахмала путем его предварительного гидролиза концентрированной НС1 [302]. В процессе гидролиза наряду с другими продуктами количественно образуется полярографически активный 5-гидроксиметилфур-фурол, волна которого и служит для аналитического определения. [c.202]
Определение крахмала [147]. Навеску исследуемого вещества кипятят с водой и затем разбавляют водой с таким расчетом, чтобы в 2 мл полученной жидкости содержалось около 10— 200 мкг крахмала. Мутные растворы фильтруют через сухой фильтр. Смешивают 2 мл фильтрата с 4 мл 0,1 %-ного раствора антрона в концентрированной Н2504. Смесь разогревается и окрашивается в зеленый и сине-зеленый цвет. После охлаждения измеряют оптическую плотность раствора при 625 нм. [c.174]
Вильдфлуш Р. Т. Сравнительная оценка методов определения крахмала в сырых материалах спиртового производства. Сб. науч. тр. (Белорус, политехи, ин-т), 1952, вып. 3, с. 261—270. 6869 [c.264]
Изосимов п. А. К вопросу, о надсернокис-лом методе определения крахмала [в зерн. продуктах]. Уч. зап. Сев.-Осет. гос. пед. ин-та, 1941, 2, вып. 2, с. 129— 134. 7281 [c.277]
Способ ускоренного определения крахмала в массе и на ткани. Н.-и. тр. (Иван. н.-и. ин-т хлопчатобумажн. пром-сти), 1951, [c.304]
Смирнов В. А. и Смирнова А. И. Об одном источнике ошибок при поляриметрическом определении крахмала в зерие. Биохимия, [c.307]
Только для арктических растений имеется приблизительное совпадение между данными сотрудника Бойсен-Йенсена Мюллера и данными Костычева и его сотрудников. Для адаптированных к сильному освещению растений умеренной зоны средняя величина, по данным датских исследователей, равна 13 мг шведских—16 мг, английских, японских и немецких (за исключением ранних работ Сакса, выполненных по методу определения крахмала в двух половинах листа) — 10 мг. Средняя величина из анализов русских ученых равна 24 мг. Результаты, полученные Костычевым, Базыриной и Васильевым [45] посредством определения синтезированных ассимилятов, не отличаются значительно от результатов, полученных ими же посредством определения поглощенной двуокиси углерода. [c.429]
При иодометрическом определении крахмал прибавляют к раствору в конце титрования, чтобы избежзть слишком сильной адсорбции (поглощения) иода крзхмзлом. Адсорбированный крахмалом иод трудно переходит в раствор, и это может вызвать ошибку в определении. [c.270]
Чтобы вычислить количество крахмала (в мг) в образце, взятом для анализа, необходимо полученный результат умножить на 40, так как для определения сахаров была взята До навески. Затем, зная навеску вещества, вычисляют процентное содержание крахмала. Наряду с крахмалом в растениях всегда присутствуют и растворимые сахара, которые переходят в водную вытяжку, реагируют с феллинговой жидкостью, и при определениях крахмала описанным выше методом получают завышенные результаты. Чтобы иметь более точные данные о содержании крахмала, необходимо в отдельной навеске определить количество редуцирующих сахаров и дисахаров и полученную величину затем вычесть из результатов определения крахмала. [c.85]
Химический анализ растений проводится для определения количества поступивших в них элементов питания, по которому можно судить о необходимости применения удобрений (методы Нейбауэра, Магницкого и др.), определения показателей пищевого и кормового достоинства продукции (определения крахмала, сахара, белка, витаминов и т. п) и для решения различных вопросов питания растений и обмена веществ. [c.282]
Гидролиз многочисленных полярографически неактивных органических соединений (целлюлозы, лигнина и других) широко применяется для их косвенного определения (подробнее см. обзор [1]). Например, было преД ложено определять малеиновый ангидрид после гидролиза его до малеиновой кислоты. Гидролиз сахарозы и рафинозы позволил определять их по волне фруктозы, глюкоза не мешает определению. Весьма перспективно определение крахмала путем гидролиза его до [c.317]
Смотреть страницы где упоминается термин Определение крахмала: [c.285] [c.163] [c.220] [c.196] [c.81] [c.231] [c.17] Смотреть главы в:
Источники:
http://vinograd.info/knigi/metodiki-po-fiziologo-biohimicheskim-issledovaniyam/kolichestvennoe-citohimicheskoe-opredelenie-krahmala.html
http://cyberleninka.ru/article/n/14599962
http://www.chem21.info/info/1694889/





