Использование свойств коллоидов в производстве вина – Коллоидные явления в винах
Использование свойств коллоидов в производстве вина – Коллоидные явления в винах
Использование свойств коллоидов в производстве вина – Коллоидные явления в винах





Определение коллоидов в сусле и вине
Производство высококачественных вин требует от винодела тонких дегустационных способностей, своеобразного таланта, расширяемого опытом. Но при всех достоинствах дегустационная оценка носит в некоторой мере субъективный и общий характер.
Дегустатор часто не в состоянии охарактеризовать роль отдельных соединений, которые влияют на органолептические качества продукта. Неудивительно, что искусство виноделия и, в частности, дегустации все больше обогащается более объективными аналитическими показателями, которые убедительно дополняют органолептические характеристики. Среди этих объективных характеристик значительную роль нужно отвести коллоидной фракции вина и сока.
Сравнение вина с живым организмом, который развивается, созревает, стареет и умирает, возможно только благодаря содержанию в нем коллоидной фракции. Коллоиды сообщают вину специфику, отличающую его от других водно-спиртовых растворов.
В то же время коллоиды имеют большое значение, как вещества, изменяющие органолептические признаки вина. Они могут стабилизировать прозрачность и цвет, придавать букету устойчивость, вызывать постепенное воздействие ароматических и вкусовых веществ на наши органы чувств и дают возможность полнее выявиться всему комплексу свойств вина, в том числе мягкости, бархатистости, гармоничности, сорбиции углекислоты (в игристом).
Изучение коллоидов вина может преследовать различные задачи. Коллоиды, как в приведенном (без сахара), так и в общем экстракте, играют (если не по количеству, то по качеству) основную роль.
Для определения степени экстрактивности вина важно знать общее количество в нем коллоидов.
При оценке сравнительной устойчивости вина против помутнения, наряду с общим количеством, нужно определять количество гидрофильных и гидрофобных коллоидов (обратимых и необратимых), а также наличие в коллоидах камеди (реакция с флорглюцином).
Поэтому значение коллоидов для виноделия трудно преувеличить.
Не меньшее значение имеет исследование коллоидов при разработке технологии соков, так как при сохранении коллоидов во многом сохраняются диетические качества сока.
Учитывая значение коллоидов для вин и соков и специфику их состава в зависимости от сорта винограда, нетрудно понять, что и в селекции винограда необходимо учитывать важную роль коллоидов.
Наконец, вино – интереснейший объект для теоретических коллоидно-химических исследований.
Для того чтобы составить наиболее полное представление о свойствах коллоидов, скажем несколько слов о дисперсных системах.
Дисперсные системы, в том числе и коллоидные, состоят из дисперсной фазы и дисперсионной среды. Дисперсная фаза сока и вина – это белковые и пектиновые вещества, камеди, растительные слизи, а также продукты дегидратации и полимеризации их и дубильных и красящих веществ. Дисперсионная среда для сока – вода, для вина – водно-спиртовая смесь.
По степени дисперсности, или по величине частиц, твердые вещества сусла и вина можно разделить на следующие фракции:
1. Макроскопическая дисперсность с поперечником частиц не менее 0,1 миллиметра. Последние представлены сильно агрегированными коллоидными хлопьями, кристаллами и агрегированными микроорганизмами, взвесь которых легко выпадает в осадок.
2. Микроскопическая дисперсность с поперечником частиц от 0,1 микрона до нескольких сотых долей миллиметра. Эти частицы представлены отдельными микроорганизмами, а также связанными в небольшие колонии, слабо агрегированными коллоидными хлопьями и мелкими кристаллами. Мельчайшие из них обладают броуновским движением, т. е. кинетически относительно устойчивы, что значительно усложняет отстой, фильтрацию, центрифугирование, различные оклейки или обработки адсорбентами. Отсюда неудачи при стерилизации методами удаления микроорганизмов.
Не менее сложна стерилизация высокими температурами, лучевой энергией, ультразвуком, так как споры или часть их надежно (за счет обезвоживания тормозных систем и оболочки) защищены от реакции на внешние воздействия. Поэтому осветление и консервирование продукта успешно осуществляется на практике только тогда, когда репродуктивные органы микроорганизмов не могут развиваться из-за отсутствия в среде одного из жизненно необходимых факторов, например кислорода, тепла, минерального или азотистого питания. На этом основан предложенный нами около 30 лет назад способ предупреждения дрожжевых помутнений столовых вин.
3. Коллоидная дисперсность с поперечником частиц от одного миллимикрона до нескольких сотых долей микрона. Такие частицы состоят из многих молекул-полимеров, обладают довольно большим объемом, сложным строением и поверхностью раздела между частицами (мицеллами) и средой.
Величина поверхностной энергии частиц имеет очень большое значение для устойчивости их размера, а также общей структуры дисперсной системы. В свою очередь, размер частиц и общая структура дисперсной системы определяют органолептические свойства сока – цвет, прозрачность, аромат, вкус.
Это положение закономерно для коллоидного состояния вещества. Известно, например, что в зависимости от размера частиц коллоидные гидрозоли серебра окрашены в синий, фиолетовый, красный или желтый цвета, в то время как ионы серебра бесцветны.
Интенсивность мутности также зависит не только от количества мутящих частиц, но и от их размера.
Изменение цвета, как правило, предшествует помутнению. Большое влияние оказывает коллоидная фракция на аромат и вкус сока. Это связано со специфическими свойствами коллоидной, полимерной, системы сока.
Полимерные частицы представлены в соке как гидрофильными, так и гидрофобными коллоидами – белковыми, а также усложненными образованиями дубильных и красящих веществ, пектином, камедью, фосфоросодержащими веществами, растительной слизью и продуктами их окисления, дегидратации и полимеризации. Все коллоидные частицы кинетически устойчивы, а гидрофильные коллоиды имеют, кроме того, связь с дисперсионной средой (растворителем).
Потеря устойчивости гидрофобных частиц (в силу присущей им тенденции к агрегации) связана с их укрупнением, а гидрофильных – с дегидратацией, главным образом в связи с окислением и последующей полимеризацией через образовавшийся кислородный мостик.
Стабилизация гидрофильного золя основана на предупреждении его окисления или же на предупреждении агрегации дегидратированных и полимеризованных частиц. Согласно нашим исследованиям * последнее достигается применением коллоида с большой защитной силой, стойкого к химическим изменениям (например, камеди плодовых культур). Так, камедь некоторых косточковых пород при применении ее в процессе окончательной фильтрации хорошо защищает соки и вина при дозировке 5-10 мг/л.
* (Авторское свидетельство № 58912)
Подбирая к дисперсной фазе подходящую дисперсионную среду и соответствующие стабилизаторы, можно любому веществу, независимо от того, является ли оно по природе кристаллическим или аморфным, придать коллоидное состояние с присущими ему свойствами.
В наиболее яркой форме свойства коллоидов проявляются при определенной степени дисперсности частиц вещества, равной 10 5 -10 7 и поперечнике их а = 10 -5 -10 -7 сантиметров.
Молекулярная дисперсность составляет примерно 10 8 , так как диаметр молекул равен 10 -8 сантиметров. Частицы диаметром 10 -5 , 10 -3 сантиметров легко различимы под микроскопом.
С изменением степени дисперсности частиц изменяются их свойства.
На рисунке 3 показана группировка веществ сока и вина по физическому состоянию (степени дисперсности). Как видно из рисунка, поверхностное натяжение (обозначено кривой σ) при степени дисперсности от микроскопической до грубоколлоидной не изменяется, а затем, при переходе к молекулярной дисперсности, резко падает и исчезает.
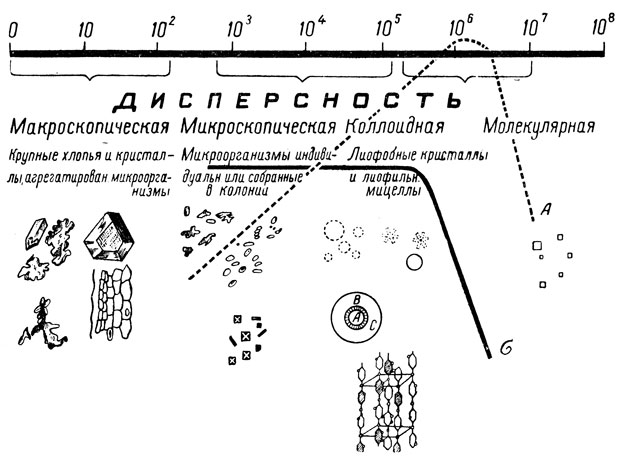
Рис. 3. Группировка веществ сока по физическому состоянию
Еще интереснее выглядит кривая удельной поверхностной энергии системы (А). Она достигает максимума у частиц с коллоидной дисперсностью.
Эти интересные зависимости были найдены А. В. Думанским в 1913 году.
Перейдем к изложению методики исследования коллоидов.
Для определения коллоидной фракции используется метод осаждения коллоидов спиртом-эфиром.
Определение общего количества коллоидов нужно начинать с нахождения оптимальной точки коагуляции по так называемому треугольнику коагуляции (рис. 4).
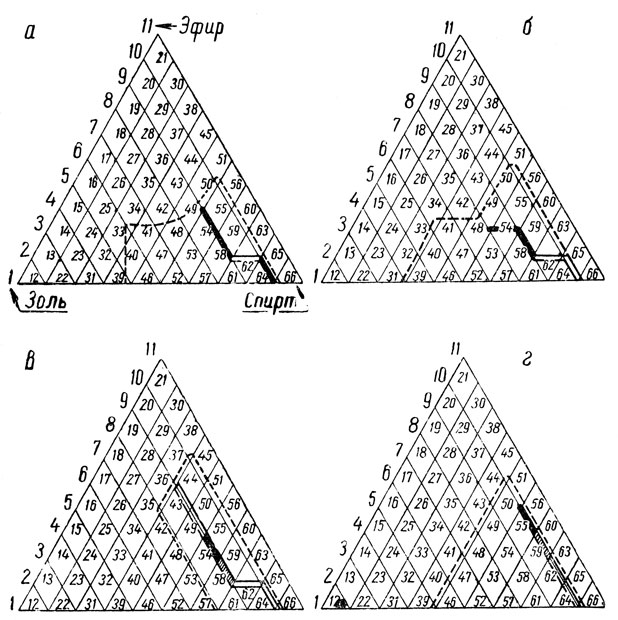
Рис. 4. Треугольники коагуляции: а, б – белых виноматериалов; в, г – красных виноматериалов
Для каждого номера системы в треугольнике соотношение золя – спирта – эфира постоянно. Это соотношение, обозначаемое порядковым номером, мы будем называть точкой треугольника коагуляции.
Каждая вершина приведенного на рисунке 4 равностороннего треугольника соответствует максимальному количеству одного из трех компонентов коагулирующей смеси, выражаемой десятью объемами.
На стороне, противоположной углу, расположены нулевые точки данного компонента.
Таким образом, отсчет производится от 10 до 0 (11 измерений), причем по мере удаления от угла к противоположной стороне количество компонента уменьшается на единицу по каждому параллельному ряду цифр.
Согласно нашим исследованиям чаще оказываются приходными следующие точки коагуляции (табл. 11):
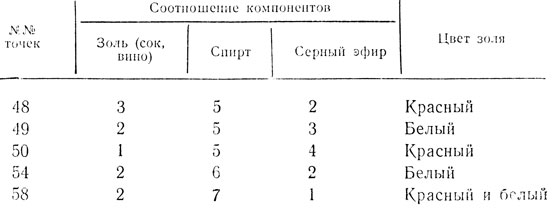
Таблица 11
Техника определения. Для осаждения коллоидов по найденной точке в конические колбочки на 100-150 миллилитров отмеривают вино, спирт, эфир в количестве, соответствующем взятой точке коагуляции, но при увеличении дозировки каждого компонента в 10 раз, чтобы смеси было 100 миллилитров (для уменьшения ошибки при пересчете). Смесь энергично взбалтывают и оставляют на ночь.
Осевший к следующему дню осадок коллоидов после декантации переносят с помощью промывной смеси для данной точки (т. е. раствора, в котором золь заменен дистиллированной водой) на беззольный фильтр, заранее высушенный и взвешенный.
При определении коллоидов в суслах с повышенной кислотностью желательно ускорять определение путем нагрева с обратным холодильником в течение 15-20 минут и фильтрования через 30-40 минут после охлаждения. Общее количество промывной смеси на каждый осадок – 70-80 миллилитров.
После промывания фильтры с осадком вкладывают в те же бюксы и помещают в водяной сушильный шкаф для определения постоянного веса, на что требуется 2-2,5 часа.
В тех случаях, когда нужно установить не только общее количество, но и количество обратимых и необратимых коллоидов, в сушильный шкаф пропускают углекислоту.
Для разделения и определения количества гидрофильных и гидрофобных коллоидов высушенный в атмосфере СО2 и взвешенный осадок коллоидов вместе с фильтром снова вкладывают в воронку и растворяют (пептизируют) теплой дистиллированной водой. Если фильтр промывать небольшими порциями теплой (45-50°) дистиллированной воды, выжидая, пока она полностью стечет, то для растворения всех гидрофильных коллоидов вполне достаточно 35-40 миллилитров воды.
Для определения количества гидрофобных коллоидов фильтр с осадком, оставшимся после пептизации гидрофильных коллоидов, вкладывают в бюкс и высушивают. По разности между весом фильтра с общим количеством коллоидов и веса его с гидрофобными коллоидами определяют количество гидрофильных коллоидов, а по разности между весом фильтра с гидрофобными коллоидами и пустого фильтра – вес гидрофобных коллоидов. Осадок гидрофобных коллоидов анализируется на общий азот, фосфор и тяжелые металлы (Fe, Pb, Cu), причем фильтрат гидрофильных коллоидов лабилен и его следует анализировать сразу, а осадок гидрофобных коллоидов можно сохранять для анализов впрок.
Полученный фильтрат идет для исследования гидрофильных коллоидов, в нем определяют физико-химические показатели – поверхностное натяжение, вязкость, Eh и химические – азот, фосфор, камеди (реакция с флорглюцином).
Основные показатели состава сусла и вина говорят не только о настоящем, но и в некоторой степени о будущем состоянии продукта. Однако, чтобы точнее прогнозировать, как изменится продукт, необходимо представлять хотя бы основные факторы или причины, с которыми связано его изменение.
Взаимодействие эномеланина с мутеобразующими коллоидными компонентами сусла и вина Текст научной статьи по специальности «Химические науки»
Похожие темы научных работ по химическим наукам , автор научной работы — Литвина Т. М., Жеребин Ю. Л.
Текст научной работы на тему «Взаимодействие эномеланина с мутеобразующими коллоидными компонентами сусла и вина»
ГЛ), фосфатидилхолин (класс ФЛ). Полученные образцы содержали также для повышения растворимости липидов альбумин (500 мг/л) и танин (1000 мг/л).
В результате ультрафильтрации модельных растворов в условиях, идентичных фильтрации виноградного сока, степень проницаемости триолеина составила 3,8%, моногалактозилдиглицерида 16,5% и фосфатидилхолина 34%, что оказалось близким к результатам, полученным на липидах виноградного сока.
Наибольшим в количественном отношении классом липидов натурального виноградного сока Одесский черный и Сухолиманский белый явились НЛ, составившие около 50%. Затем в порядке уменьшения содержания следовали ГЛ и ФЛ (табл. 1).
Групповой состав липидов сока Сухолиманский белый представлен в табл. 2. Превалирующими типами липидных соединений являлись эфиры стеринов, триацилглицерины, свободные стерины, эфиры жирных кислот, цереброзиды, гликозиды стеринов, керамидолигозиды, фосфатидилэтаноламины, фос-фатидилглицерины и фосфатидилхолины. Групповой состав липидов соков обоих сортов был весьма близок. Следует отметить, что в процессе ультрафильтрации качественный состав и количественное соотношение липидов сока менялось незначительно. Лишь во фракции нейтральных липидов нами отмечена высокая степень (до 99%) задерживания эфиров стеринов и эфиров жирных кислот. Это свидетельствует о том, что в пределах отдельного класса липидов не наблюдается выраженной селективности в удалении отдельных групп при мембранной фильтрации.
Однако ультрафильтрационное ответление дает возможность удалить основную массу нейтральных липидов, участвующих в формировании помутнений и развитии окислительных процессов в соках, и частично сохранить полярные липиды, доля.которых после обработки уже составляет
Следовательно, с помощью ультрафильтрации можно устранить из сока не только нерастворимые шламовые вещества, но и снизить содержание веществ как липидной, так и белковой, полифеноль-ной и полисахаридной природы, вызывающих дестабилизацию соков.
Полученные по приведенной схеме образцы осветленных соков отличались кристаллической прозрач-
ностью с блеском, высокой стабильностью, хор шими органолептическими свойствами.
Таким образом, с учетом полученных экспериме тальных данных разработана схема ультрафильтр ционного осветления виноградного сока с испол зованием половолоконного мембраннного моду. АР-2, которая внедряется на заводе продтовар« № 2 г. Одессы и опытном заводе УНИИВВ и В. Е. Таирова. Ожидаемый экономический эффе от внедрения составляет свыше 30 тыс. р. в го
1. Фисенко В. Ю., Ажогина В. А., Фисе
ко В. Н., Ивлев П. Ф. Влияние липидов вин градной ягоды и вина на формирование качества бел] столовых вин//Изв. вузов. Пищевая технология. 1977,— № 1,— С. 86—89.
2. Богатский А. В., Жеребин Ю. Л., Коле
ник А. А., Тюрин С. Т. Липиды как эндогенн)
антиоксиданты вин и виноматериалов//СадоводстЕ виноградарство и виноделие Молдавии.— 1979.
3. Мехуэла Н. А., Курганова Г. В., Нага
чук В. В. Способы предупреждения обратим! коллоидных помутнений вин//Науч.-техн. реф. сб. В нодельческая пром-сть.—1983.— № 1.— С. 1—4.
4. Богатский А. В., Жеребин Ю. Л., Коле ник А. А. Липиды вина и быстрый метод их выл ления//Виноградарство и виноделие СССР.—1978. № 8, — С. 26—29.
5. Жеребин Ю. Л., Колесник А. А., Бога с кий А. В. Полярные липиды вина//Прикладн биохимия и микробиология.—1981.—17.— Вып, 4. С. 614—620.
6. Жеребин Ю. Л., Колесник А. А., Бога с к и й А. В. Исследование липидов некоторых со тов ягод винограда ‘в процессе созревания//Физи логия и биохимия культурных растений.— 1984.—16. № 3,— С. 243—248.
7. Богатский А. В., Жеребин Ю. Л., Коле
НИК А. А. Количественное Определение ЛИПИДН1 фракций сусел и вин//Виноделие и виноградарст СССР,—1980,—№ 6,—С. 21—24.
8. Жеребин Ю. Л., Колесник А. А. Фитогл колипиды винограда//Химия природных соединений. 1984,— № 3.—С. 296—300.
9. Жеребин Ю. Л., Колесник А. А. Фосфолипщ виноградной ягоды.— Химия природных соединений. 1984,— № 2,—С. 165—168.
Использование свойств коллоидов в производстве вина – Коллоидные явления в винах
КОЛЛОИДНЫЕ СИСТЕМЫ В ПИЩЕВЫХ ПРОИЗВОДСТВАХ
Коллоидное состояние характеризуется следующими основными признаками: определенными размерами частиц (10 -7 . 10 -5 см), гетерогенностью и многокомпонентностью.
Дисперсные системы с частицами коллоидных размеров принято называть золями (от латинского слова solutio — раствор).
Системы с газовой дисперсионной средой независимо от природы газа называют аэрозолями. Системы с жидкой дисперсионной средой — лиозолями (от греческого слова lios — жидкость). В зависимости от природы жидкости лиозоли называют гидрозолями (вода), органозолями (органическая среда) или более конкретно — алкозолями (спирты), этерозолями (эфиры) и т. д.
По размеру частиц золи занимают промежуточное положение между истинными растворами и грубодисперсными системами — порошками, суспензиями и эмульсиями. Коллоидные системы образуются двумя путями: диспергированием — дроблением
крупных частиц грубодисперсных систем до коллоидной дисперсности; конденсацией — соединением атомов ионов или молекул в более крупные частицы коллоидных размеров. При этом необходимыми условиями образования коллоидных систем являются нерастворимость вещества дисперсной фазы в дисперсионной среде; достижение частицами дисперсной фазы коллоидной дисперсности; наличие стабилизатора, сообщающего коллоидной системе агрегативную устойчивость.
Стабилизаторами могут быть вещества, специально вводимые в дисперсионную среду, например поверхностно-активные вещества или продукты взаимодействия дисперсной фазы с дисперсионной средой. Стабилизаторы создают вокруг коллоидных частиц адсорбционный защитный слой, препятствующий их агрегатированию.
В производстве различных пищевых продуктов диспергирование и конденсация занимают одно из ведущих мест. Это обусловлено особенностями вещества в дисперсном состоянии, которые обеспечивают удобства фасования, транспортирования, дозирования, способствуют увеличению скоростей химических и биохимических реакций и процессов растворения, сорбции, экстракции и других процессов.
Диспергирование используют при дроблении и измельчении зерна в муку, какао-бобов в какао тертое и какао-порошок, сахара в сахарную пудру, в консервной промышленности при гомогенизации плодово-ягодных пюре и т. п.
Конденсация возникает в ректификационных аппаратах при получении спирта, кристаллизации сахара, выпаривании растворов, оклейке вин и т. д.
Коллоидные системы обладают молекулярно-кинетическими свойствами, обусловленными самопроизвольным движением частиц. Это такие свойства, как диффузия, осмотическое давление и распределение частиц по высоте.
Причиной диффузии (самопроизвольное выравнивание концентраций) частиц в коллоидных системах является броуновское движение, которое, в свою очередь, является следствием геплово-го движения молекул дисперсионной среды. Скорость диффузии обратно пропорциональна размеру диффундирующих частиц, поэтому в коллоидных системах, частицы которых имеют размеры порядка 10_7. 10
5 см, т. е. значительно больше молекул обычных низкомолекулярных веществ, скорость диффузии невелика.
На коллоидные частицы, распределенные в дисперсионной среде, действуют две противоположно направленные силы: сила тяжести и сила диффузии. Под действием силы тяжести частицы стремятся осесть на дно — седиментировать (от латинского слова sedimentum — осадок). Силы диффузии же стремятся распределить частицы равномерно по всему объему системы. Таким образом, дисперсные системы способны сохранять определенное распределение частиц по объему. Эта способность называется седиментиционной или кинетической устойчивостью. Грубодисперсные системы кинетически неустойчивы, их частицы велики и поэтому под действием силы тяжести оседают на дно. Молекулярные системы (газы, растворы) обладают очень высокой кинетической устойчивостью. Кинетическая устойчивость коллоидных систем зависит от размеров их частиц: чем меньше размер частиц, тем более кинетически устойчива коллоидная система.
МИКРОГЕТЕРОГЕННЫЕ СИСТЕМЫ В ПИЩЕВЫХ ПРОИЗВОДСТВАХ
К микрогетерогенным системам с размером частиц 10
5. 1СГ3 см относят суспензии (Т/Ж), эмульсии (Ж/Ж), пены (Г/Ж), аэрозоли (Т/Г и Ж/Г) и порошки (Т/Г). Как правило, эти системы непрозрачны, частицы гетерогенных систем быстро оседают. Все эти системы широко распространены в природе и имеют большое значение в пищевой промышленности.
Суспензии. Представляют собой дисперсные системы с твердой дисперсной фазой и жидкой дисперсионной средой. К ним относятся фруктовые и овощные пасты, помадные конфетные массы, какао тертое и др.
Суспензии имеют ряд общих свойств с порошками; эти системы подобны им по дисперсности. В пищевой промышленности суспензии образуются при получении крахмала, при осаждении осадков в производстве сахара, пива, вина, в кондитерской промышленности и др.
Эмульсии. Дисперсные системы, состоящие из жидкой дисперсной фазы и жидкой дисперсионной среды, называются эмульсиями. Обязательное условие образования эмульсии — нерастворимость вещества дисперсной фазы в дисперсионной среде.
Обычно эмульсии получают методом механического диспергирования. Для этого используют различные мешалки, смесители, гомогенизаторы, коллоидные мельницы и ультразвук.
Жидкости, из которых получают эмульсии, нерастворимы друг в друге и, следовательно, отличаются по своим свойствам.
Практически одной из жидкостей всегда является вода, а другой — какая-либо неполярная, нерастворимая в воде жидкость, например масло.
Эмульсии — неустойчивые системы. Неустойчивость этой системы проявляется в самопроизвольном слиянии капелек дисперсной фазы — коалесценции, что приводит к разрушению эмульсии и разделению ее на два слоя. Устойчивость эмульсиям может придать только третий компонент — стабилизатор или эмульгатор. Роль эмульгатора в образовании устойчивой эмульсии заключается, во-первых, в том, что он адсорбируется на границе раздела фаз масло — вода (М/В) и снижает межфазное поверхностное натяжение, т. е. является поверхностно-активным веществом, а во-вторых, концентрируясь на поверхности капелек дисперсной фазы, эмульгатор образует механически прочный слой (пленку). Наличие такой защитной пленки на поверхности частиц дисперсной фазы препятствуют их слиянию, т. е. предохраняет эмульсию от коалесценции.
Природа эмульгатора определяет не только устойчивость, но и тип эмульсии. Эмульгаторы, растворимые в воде, способствуют образованию прямых эмульсий (М/В); эмульгаторы, растворимые в неполярных жидкостях, дают обратные эмульсии (В/М).
К представителям эмульсий относится ряд важнейших жиросодержащих продуктов, например молоко, сливки, сливочное масло, сметана и майонез. Все это — эмульсии. Жиры — необходимая составная часть продуктов питания, но так как они нерастворимы в воде, то лучше усваиваются в эмульгированном состоянии. Поэтому употребляемые в пищу жидкие или твердые жиры (растительное масло, животные жиры) в организме сначала переводятся в эмульгированное состояние под действием желчи, а потом усваиваются.
Аэрозоли и порошки. Это дисперсные системы, дисперсионной средой которых является газ (воздух), а дисперсной фазой могут быть твердые частицы или капельки жидкости. Обычно аэрозоли классифицируются по агрегатному состоянию дисперсной фазы. Аэрозоль с жидкой дисперсной фазой называют туманом, с твердой — дымом и пылью. Аэрозоли с твердой дисперсной фазой, размеры частиц которой больше, чем у дымов, называют обычно пылью. Это деление достаточно условно. Размеры частиц аэрозолей лежат в пределах от 10 -5 до 10 -2 см. Аэрозоли имеют большое практическое значение в ряде отраслей пищевой промышленности. К типичным аэрозолям относятся водяной туман, топочный дым, мучная и сахарная пыль. В ряде случаев в промышленности прибегают к искусственному получению аэрозолей. Так, для высушивания соки, пюре, молоко распыляют до мельчайших капелек в сухом горячем воздухе. Из образующегося аэрозоля благодаря его большой удельной поверхности испарение влаги идет очень интенсивно и сушка заканчивается за 15. 20 с.
Образование аэрозолей может привести к нежелательным и опасным последствиям. Так, пыль многих веществ — муки, сахара, крахмала, угля — образует с воздухом взрывоопасные смеси.
Порошки можно рассматривать как осажденные аэрозоли с твердыми частицами. Однако частицы в них могут быть более крупными и достигать в диаметре 1. 2 мм. Размер частиц промышленных порошков определяется их целевым назначением и часто является одним из основных показателей качества продукта. Например, дисперсность и распределение частиц по размерам в какао-порошке влияют на вкусовые качества и пищевую ценность этого продукта. Степень помола зерна оказывает влияние на качество муки.
Частицы порошка всегда находятся в контакте и по этой причине имеют свойство текучести, которое, в свою очередь, зависит от плотности, размера и формы частиц, состояния их поверхности, влажности и других свойств. Повышение дисперсности приводит к уменьшению текучести вследствие роста общей поверхности контакта. Увеличение влажности также снижает текучесть порошков.
Пены. Высококонцентрированные дисперсные с.истемы, в которых дисперсионная среда — жидкость, а дисперсная фаза — газ, называются пенами. Пузырьки газа в пенах имеют большие размеры, форму многогранников и отделены друг от друга очень тонкими слоями дисперсионной среды. Для получения пен применяют диспергационные методы: интенсивное встряхивание или перемешивание жидкости.
Устойчивую пену можно получить только в присутствии стабилизатора — пенообразователя. Это связано с тем, что поверхность жидкости, соприкасающаяся с газообразной средой, находится в особых условиях по сравнению с основной массой жидкости. Эти условия возникают потому, что молекулы поверхностного слоя жидкости в отличие от молекул, находящихся в глубине, подвергаются неодинаковому притяжению молекул жидкости и газа. Каждая молекула внутри жидкости со всех сторон притягивается соседними молекулами, расположенными на расстоянии радиуса сферы действия межмолекулярных сил (рис. 36). В результате силы притяжения компенсируются и равнодействующая этих сил равна нулю.

Рис. 36. Схема возникновения поверхностного натяжения:
1 — молекулы; 2 — сферы действия межмолекулярных сил

Рис. 37. Схема структуры пены
У молекул поверхностного слоя часть сферы действия межмолекулярных сил находится в газовой фазе, плотность которой меньше плотности жидкости, поэтому равнодействующая всех сил притяжения будет направлена внутрь жидкости перпендикулярно к ее поверхности. Вследствие этого поверхностные молекулы жидкости всегда находятся под действием силы, стремящейся втянуть их внутрь. Это приводит к тому, что поверхность жидкости всегда стремится сократиться. Этим объясняются и шарообразная форма капли жидкости (шар имеет минимальную поверхность), и идеально гладкая поверхность жидкости в широком сосуде. При увеличении поверхности некоторое число молекул из глубины жидкосги переходит на поверхность. Процесс переноса молекул из равновесного состояния в особое состояние молекул поверхностного слоя требует затраты внешней работы. Работа по увеличению площади поверхности жидкости переходит в потенциальную энергию молекул поверхностного слоя — поверхностную энергию. Последняя, в свою очередь, отнесенная к единице поверхности, называется поверхностным натяжением
где F— поверхностная энергия; .V — площадь поверхности.
Пенообразующие вещества с длинной молекулярной цепью уменьшают поверхностное натяжение, облегчают образование пены и придают ей стабильность, так как они адсорбируются на границе вода — воздух и образуют высоковязкую структурированную пленку, препятствующую сгеканию жидкости (рис. 37). В этом случае толщина слоя жидкости между пузырьками воздуха уменьшается медленно и пена может существовать длительное время.
Пенообразователями могут служить поверхностно-активные вещества (ПАВ), молекулы которых имеют достаточно длинную углеводородную цепь. Многие молекулы органических веществ состоят из двух частей: полярной группы и неполярного углеводородного радикала. К полярным группам относятся —СООН,
-ОН, -NH, —SH, -CN и т. д. Эти группы гидрофильны, т. е. хорошо смачиваются водой. В отличие от них углеводородные радикалы гидрофобны, т. е. не смачиваются водой. Схематически дифильные, состоящие из гидрофильной и гидрофобных частей молекулы изображают в виде символа —•, в котором прямой чертой обозначают неполярный радикал, а кружком — полярную группу.
К типичным пенообразовате-иям водных пен относятся спирты, мыла, белки. Пенообразова-иие имеет важное практическое значение. В частности, многие продукты, такие, как хлеб и ряд кондитерских изделий, имеют структуру пены, что определяет их вкусовые свойства и пищевую ценность.
Источники:
http://wine.historic.ru/books/item/f00/s00/z0000037/st011.shtml
http://cyberleninka.ru/article/n/vzaimodeystvie-enomelanina-s-muteobrazuyuschimi-kolloidnymi-komponentami-susla-i-vina
http://zinref.ru/000_uchebniki/04200produkti/006_00_tehnologia_pishevih_proizvodstv_kovalskaia_1997/022.htm




