Электрический заряд частиц – Коллоидные явления в винах
Электрический заряд частиц – Коллоидные явления в винах
Коллоидные явления в винах – Электрический заряд частиц
Содержание материала
Существование электрического заряда частиц констатируют, пропуская через коллоидный раствор постоянный электрический ток. 
Рис. 11.6. Электрофорез (частицы заряжены положительным электричеством). Выше коллоидного раствора находится чистый растворитель.
Частицы переносятся к одному или другому электроду. При этом, если перемещение наблюдается простым глазом, то речь идет о помутнении; или же оно определяется химическим количественным анализом коллоидного вещества, находящегося около каждого электрода. Это — явление электрофореза (рис. 11.6). Если частицы перемещаются к аноду, они заряжены отрицательно; в этих случаях говорят, что коллоид электроотрицательный, и наоборот. Эти понятия применяются к суспензиям и к гидрофобным коллоидам. Так, коллоидный: краситель, фосфат железа, железисто-синеродистое железо, сульфат меди, диатомит, каолин, бентонит заряжены отрицательно даже в такой кислой среде, как вино (рН 3), где значительно преобладают ионы Н+ над ионами ОН-; и наоборот, целлюлоза, гидроокись железа заряжены положительно.
Для объяснения заряда частиц было предложено несколько теорий. По физической теории электрический заряд образуется в результате адсорбции на поверхности частиц ионов из раствора или анионов, сообщающих частице отрицательный заряд, или катионов, которые сообщают ей положительный заряд (рис. 11.7).
Во всех случаях, когда осуществляется контакт между твердым телом и жидкостью, в зоне их соприкосновения возникают два электрических слоя с противоположными знаками, (двойной электрический слой). При этом один из них примыкает к твердому телу, которому он сообщает свой знак, другой же образуется тонким слоем жидкости, окружающим твердое тело, и обеспечивает нейтральность всего комплекса. Точнее, вокруг частицы или оболочки находится некоторый объем, нечто вроде «атмосферы», в которой преобладают ионы ( + ) или ионы (—), причем их избыток уменьшается по мере удаления от оболочки. В сущности, никакого двойного слоя нет, но наряду с ионами, фиксированными на такой оболочке, имеется как бы рассеянный слой — ионная атмосфера оболочки (рис 11.8). На некотором удалении ионы ( + ) и ионы (—) распределены равномерно в эквивалентной численности и более или менее перемешаны с ионами раствора, наиболее удаленными от ионной атмосферы, что на рисунке не показано.
Частицы, взвешенные в чистой воде при рН 7, которая включает катионы Н+ и анионы ОН- в эквивалентных количествах, обычно покрыты слоем ионов. ОН-, который сообщает им отрицательный заряд; в совокупности они
представляют собой крупный радикал кислого характера, насыщенный внешними ионами Н+. Частицы, взвешенные в вине, которое содержит немного больше ионов Н+, чем ионов ОН
(рН 3), имеют тенденцию фиксировать меньше ионов ОН-, чем в чистой воде, или даже фиксировать ионы Н+ и принимать положительный заряд; фиксации ионов Н+ способствует их относительно высокая концентрация.
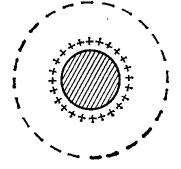
Рис. 11.7. Схематическое изображение двойного слоя вокруг электроположительной частицы. 
Рис. 11.8. Ионная атмосфера.
Между высокими рН, которые сообщают отрицательный заряд, и низкими рН, сообщающими положительный заряд, существует некоторый рН, так называемая изоэлектрическая точка, где заряд, равен О. Изоэлектрический рН обычно не совпадает с нейтральностью (рН 7).. Ионы Н+ и ОН- не единственные, которые могут фиксироваться коллоидными частицами, хотя их действие обычна бывает преобладающим. Следовательно, различные анионы и катионы раствора в большей или меньшей мере фиксированы: поливалентные ионы могут менять знак, сообщенный ионами Н+ или ОН-. Для получения стабильности частица должна фиксировать положительные или отрицательные ионы, следовательно, жидкость должна содержать некоторое количество электролитов. Если из раствора удалить посредством диализа все электролиты, произойдет флокуляция.
Таким образом, эта теория включает ионную адсорбцию. Фиксируются наиболее адсорбируемые ионы и те, которые содержатся в наибольшей пропорции. Но частицы часто состоят из микрокристаллов и случается, что просто один из ионов, образующих эти микрокристаллы, оказывается лишним. Он входит в микрокристаллическую решетку и находится на поверхности микрокристалла в точно определенном положении. Не все микрокристаллы обязательно нейтральные, и лишний ион дает микрокристаллу свой собственный знак. Результат тот же, как и при ионной адсорбции.
Разработаны и другие концепции о составе и структуре гидрофобных коллоидов. Их свойства легче объяснить, если допустить, что атомы образуют в них правильную кристаллическую решетку, прерываемую нарушениями структуры, которые представляют собой точки связи между молекулой и внешней средой и точки воздействия реактивов. Именно эти разрывы в некоторых случаях в большей степени ответственны за растворимость и стабильность коллоидов, чем поверхностные явления и ионная адсорбция.
Согласно химической теории заряд имеет химическую природу: коллоидные частицы ведут себя как молекулы электролитов. Так же как в растворе, молекула NaCl разлагается на две части: один или несколько простых ионов обычного размера и крупный ион значитательно большего размера, который бывает анионом или катионом.
Например, частица золя сульфата меди отрицательного коллоида состоит из молекулы сероводорода, ассоциированной с некоторым числом молекул сульфата меди и, следовательно, может быть записана как (CuS)„-H2S. Эта частица разлагается в жидкости, как молекула, давая два иона Н+ и один крупный комплексный ион, заряженный отрицательно, т. е. (CuS)„-S__. Также крупный комплексный ион гидроокиси железа (положительный коллоид) будет, например, в присутствии ионов СЬ иметь вид (Fe(OH3)„Fe+++. Возрастание размера частиц, связанное с увеличением числа п и ведущее к флокуляции, видимо, обусловлено химическими реакциями. Эти реакции касаются в первом случае только радикала H2S, составляющего активную часть частицы, или же во втором случае оно ведет к удалению посредством диализа электролитов из раствора, вызывая отделение ионов Fe+++ от частицы и увеличение п. Заряд здесь обязан не «ионной адсорбции, а ионизации активной молекулы или «поверхностной ионизации».
Механизм возникновения заряда в коллоидных частицах. Строение двойного электрического слоя. Мицелла, гранула, ядро.
При воздействии на дисперсную систему электрического поля можно наблюдать перемещение дисперсной фазы относительно дисперсионной среды. Следовательно, части дисперсионной системы электрически заряжены. Движение частиц в электрическом поле было названо электрофорезом, а движение растворителя – электроосмосом.
Возникают разные потенциалы как при перемещении дисперсионной среды относительно неподвижной дисперсной фазы – потенциал протекания, так и наоборот, при перемещении дисперсной фазы относительно неподвижной дисперсионной среды – потенциал седиментации.
Перемещение дисперсной фазы или дисперсионной среды под действием внешнего электрического поля или возникновения разности потенциалов при перемещении дисперсной фазы и дисперсионной среды друг относительно друга н-ся электрокинетическими явлениями.
Прицина эл.кин явленй – об-ние двойного эл-кого заряда как у частиц дисперсной фазы, так и у дисперсионной среды.
Электрический заряд на границе раздела фаз может возникать в р-те избирательной адсорбции одного из ионов растворенного электролита, или вследствии диссоциации поверхностных молекул в-ва дисперсионной фазы. В р-те этих процессов на границе раздела фаз возникает двойной электрический слой.
ДЭС состоит из достаточно прочно связанных с поверхностью дисперсионной фазы потенциалопределяющих ионов и эквивалентного к-ва противоположно заряженных ионов – противоионов, находящихся в дисперсионной среде.
Расположение противоионо в д. среде определяется двумя противоположными факторами: тепловое движение стремиться распределить ионы по всему объему жидкой фазы, а силы электростатического напряжения стремятся удержать их вблизи поверхности раздела фаз. В р-те этих факторов устанавливается диффузионное распределение противоинов с уменьшающейся концентрацией по мере удаления от межфазной границы. Необходимо так же учитывать возможность адсорбционного взаимодействия противоионов с поверхностью дисперсной фазы, Вследствие адсорбционного взаимодействия и электростатического притяжения часть противоионов оказывается прочно связанной с дисперсионной фазы. Потенциалопределяющие ионы вместе со связанными противоионами образуют адсорбционный слой небольшой толщины. Оставшаяся часть противоионов образует диффузный слой с убывающей концентрацией.
Строение мицелл. Согласно современным представлениям коллоидные частицы представляют собой образования со сложной структурой – мицеллы. Мицелла состоит из электронейтрального агрегата и ионногенной части. Масса кооидной частицы гл образом сосредоточена в агрегате, который состоит из сотен атомов и молекул.
Агрегат может иметь как аморфное, так и кристаллическое строение. ионогенная часть мицеллы делится на адсорбционный и диффузный слои.
Агрегат в результате избирательной адсорбции ионов или оинизации поверхностных молекул приобретает заряд. Ионы, определяющие заряд агрегата – потенциалопределяющие. Агрегат + ПОИ = ядро. .С заряженной поверхностью ядра устойчиво связано некоторое число ионов противоположного знака – противоионов . ПОИ + противоионы = адсорбционный слой. агрегат + адсорбционный слой = гранула. Заряд гранулы равен сумме зарядов противо и ПОИ
Электрический заряд частиц – Коллоидные явления в винах

Здесь U– скорость движения или подвижность частиц,ε- диэлектрическая проницаемость среды, Е – напряженность внешнего электрического поля,ζ- электрокинетический потенциал,η- вязкость раствора.
Уравнение Смолуховского справедливо для достаточно крупных коллоидных частиц с приблизительно шарообразной формой, таких как клетки крови, вирусы и некоторые бактерии. Для небольших коллоидных частиц, соответствующих по размерам отдельным молекулам белков, высокомолекулярных соединений, скорость электрофорез сильно зависит от различий в длине и ширине. Она определяется для таких случаев уравнением Дебая и Гюккеля:
Здесь К – коэффициент, величина которого зависит от формы частиц.
Скорость электрофореза, отнесенная к единице напряженности электрического поля, называется электрофоретической подвижностью:
Здесь V– электрофоретическая подвижность.
Электрофоретическую подвижность определяют экспериментально в специальных микрокамерах, наблюдая в микроскоп. Это позволяет рассчитать дзета-потенциал коллоидных частиц, что необходимо для определения числа заряженных группировок и природы их поверхности. Электрофорез широко используется в медико-биологических исследованиях для разделения аминокислот, белков, нуклеиновых кислот, форменных элементов крови с целью выделения этих веществ и диагностирования заболеваний.
В ходе электрофореза противоионы диффузионного слоя коллоидных частиц обычно вовлекают в свое движение окружающую массу растворителя вследствие их сольватации. Однако это движение растворителя не является направленным, оно приводит просто к перемешиванию раствора. Если заряд возникает и на неподвижной поверхности, то движение противоионов над ней вызывает направленное перемещение всего раствора в сторону электрода, заряд которого противоположен заряду противоионов. Поэтому наложение внешней разности потенциалов, на пористые среды, содержащие воду, такие как почва, рыхлые осадки, древесина, бетон, кирпич приводит к просасыванию водного раствора через капилляры пористой среды. По этой причине и происходило повышения уровня раствора в катодной трубке в опыте Рейсса. Явление перемещения раствора через капилляры пористой среды под действием внешнего электрического поля к электроду, заряд которого противоположен заряду противоионов по аналогии с осмосом было названо электроосмосом. Электроосмос используется для ускорения фильтрации, осушения рыхлых осадков лекарственных веществ в фармацевтической промышленности.
Источники:
http://vinograd.info/knigi/teoriya-i-praktika-vinodeliya/kolloidnye-yavleniya-v-vinah-8.html
http://studopedia.ru/19_369404_mehanizm-vozniknoveniya-zaryada-v-kolloidnih-chastitsah-stroenie-dvoynogo-elektricheskogo-sloya-mitsella-granula-yadro.html
http://studfile.net/preview/4022374/page:4/





