Антоцианы – Фенольные соединения
Антоцианы – Фенольные соединения
Фенольные соединения
К фенольным соединениям ФС относится обширный класс циклических веществ, являющихся производными ароматического спир- та фенола (С6Н5ОН). В молекуле фенольных соединений имеется ароматическое кольцо, содержащее одну или несколько гидроксильных групп. Фенольные соединения находятся в растениях, плодах и овощах преимущественно в виде гликозидов и реже в свободном виде [24].
Биосинтез фенольных соединений в растительной клетке происходит в протоплазме, в частности, в хлоропластах. Однако основная масса водорастворимых фенолов сосредоточена в вакуолях, ограниченных от цитоплазмы белково-липидной мембраной тонопластом, который регулирует участие веществ, содержащихся в вакуолях, в метаболизме клетки. В животном организме фенольные соединения не синтезируются, а поступают с растительной пищей и участвуют в обменных процессах.
К гликозидам относятся разнообразные вещества, у которых какой-либо сахар (чаще глюкоза, реже другие моносахариды) соединен за счет гликозидного гидроксила с другими веществами, не являющимися сахарами (спиртами, альдегидами, фенолами, алкалоидами, стероидами и др.). Вторая часть молекулы гликозидов называется агликоном (не сахар).
От содержания и превращений фенольных соединений зависят цвет и аромат плодов, качество чая, кофе, вина. Многие фенолы обладают свойствами витамина Р и являются антиоксидантами.
Все фенольные соединения являются активными метаболитами клеточного обмена и играют важную роль в различных физиологических функциях растений, плодов, картофеля и овощей дыхании, росте, устойчивости к инфекционным заболеваниям.
О важной биологической роли фенольных соединений свидетельствует их распределение в растительной ткани. Разные органы и ткани растений, плодов и овощей различаются не только количественным содержанием фенолов, но и качественным их составом.
В настоящее время известно более 2000 фенольных соединений, существенно различающихся по своим свойствам. В связи с этим важное значение имеет классификация фенольных соединений.
Фенольные соединения условно разделяются на три основные группы:
Мономерные фенольные соединения содержат одно ароматиче-ское кольцо и делятся на три подгруппы:
соединения С6-ряда, состоящие из ароматического кольца без углеродных боковых цепей; к ним относятся гидрохинон, пирокатехин и его производные, гваякол, флороглюцин, пирогаллол. Все они содержатся в растениях главным образом в связанном виде;
соединения с основной структурой С6С1-ряда включают в себя группу фенолкарбоновых кислот и их производных протокатеховую, ванилиновую, галловую, салициловую, оксибензойную и другие кислоты; эти соединения встречаются в плодах и овощах в свободном виде;
соединения с основной структурой С6С3-ряда, состоящие из ароматического кольца и трехуглеродной боковой цепи, делятся на коричные кислоты, кумарины и производные последних: изокумарины, фурокумарины.
Кумарины рассматриваются как лактоны оксикоричных кислот. Наиболее распространенными коричными кислотами являются п-ку-маровая, кофейная, феруловая и синаповая.
Фенолкарбоновые кислоты, обладая фенольными и кислотными группами, могут реагировать друг с другом с образованием соединений типа сложных эфиров, называемых депсидами. Если в реакции участвуют две фенолкарбоновые кислоты, то образуется дидепсид, если три тридепсид и т.п. Соединения С6С3-ряда участвуют в формировании аромата и вкуса плодов и овощей.
Димерные фенольные соединения имеют основную структуру с двумя ароматическими кольцами С6С3С6 и делятся на флавоноиды и изофлавоноиды (ротеноиды). Эти соединения наиболее широко распространены в природе, и многие из них принимают участие в формировании аромата и цвета растительных продуктов.
В зависимости от структуры связующего трехуглеродного фрагмента в молекуле и степени окисленности флавоноиды подразделяются на катехины, лейкоантоцианы, флаваноны, флаванонолы, антоцианы, флавоны, флавонолы и другие. Наиболее восстановленные соединения катехины, наиболее окисленные флавонолы.
Катехины бесцветные соединения, легко окисляются, в результате чего приобретают разную окраску. Например, различный цвет чая (черный, красновато-коричневый, желтый) обусловлен степенью окисления катехинов, содержащихся в чайном листе. Существует несколько форм катехинов: катехин, галлокатехин, галлокатехингаллат и другие. Каждый катехин может существовать в виде четырех оптических изомеров, различающихся по направлению и величине угла вращения: (+)-катехин, ()-катехин; (+)-эпикатехин, ()-эпикатехин. Кроме того, для каждого катехина известны два рацемата смесь, лишенная оптической активности: (+)-катехин и (+)-эпикатехин. Все они отличаются по физическим свойствам и биологическому действию. Например, высокой Р-витаминной активностью обладает ()-эпикатехин.
В плодах и овощах катехины могут присутствовать в свободном и связанном состоянии (в составе полимерных форм). Много катехинов содержится в винограде, айве, черной смородине, яблоках, черноплодной рябине, косточковых плодах и ягодах.
Катехины хорошо растворимы в воде, имеют слабый вяжущий вкус, легко окисляются на свету, при нагревании, особенно в щелочной среде под действием окислительных ферментов (фенолоксидазы и пероксидазы). Продукты окисления хиноны и полимеризации катехинов флобафены придают плодам и овощам при термической и механической обработке темную окраску.
Окисление фенольных соединений может быть обратимым и необратимым. Этот процесс происходит и в здоровых, неповрежденных растительных клетках, но ткань их при этом не темнеет. Это обусловлено тем, что через тонопласт в цитоплазму поступает строго ограниченное количество фенолов, рассчитанное на тот ферментативный аппарат, который имеется в цитоплазме.
При окислении в здоровой клетке часть фенолов окисляется до карбоновых кислот и в качестве конечных продуктов окисления образуются СО2 и Н2О.
Часть же промежуточных продуктов окисления фенолов с помощью ферментов фенолоксидазы и пероксидазы, а также восстановителей, вновь восстанавливается до исходных соединений.
В поврежденных клетках в контакте с о-фенолоксидазой оказывается сразу большое количество фенолов и поэтому восстановления не происходит, а образующиеся хиноны необратимо конденсируются как между собой, так и с аминокислотами с образованием коричневых и красных аморфных веществ флобафенов.
Например, причиной потемнения очищенных и нарезанных клубней картофеля является окисление аминокислоты фенольного ха-рактера тирозина (-оксифенилаланин). Тирозин окисляется до диоксифенилаланина, который превращается в хинон, образующий красные гетероциклические соединения. Хиноны полимеризуются и превращаются в продукты темного цвета меланины.
Образование темноокрашенных веществ при хранении очищенного картофеля может происходить в результате окисления другого вещества фенольной природы хлорогеновой кислоты. Потемнение внутренней сердцевины картофеля связано с окислением хлорогеновой кислоты, а внешней сердцевины с окислением тирозина.
Предотвратить окисление фенолов очень важно при производстве крахмала, так как образующийся при измельчении картофеля клеточный сок содержит наряду с другими веществами тирозин. Последний легко окисляется, что вызывает потемнение крахмала, ухудшение его качества. Быстрое отделение клеточного сока от крахмала на центрифуге позволяет получить крахмал высокого качества.
Для предотвращения потемнения плодов и овощей при чистке, резке и дроблении применяют различные вещества (диоксид серы, аскорбиновую, лимонную кислоты и др.), а также тепловую обработку для инактивации фенолоксидаз, пероксидаз и каталазы.
На предприятиях общественного питания применяется сульфитация очищенного картофеля, заключающаяся в обработке клубней слабым раствором диоксида серы (0,10,2%).
Лейкоантоцианы, флаваноны и флаванонолы это бесцветные фенольные соединения. Лейкоантоцианы изменяют окраску в зависимости от температуры. Так, при 135С они имеют желтый цвет, при 165С винно-красный, выше 225С сине-серый, при 260С черный. При нагревании они превращаются в лейкоантоцианидины. Лейкоан-тоцианы в значительном количестве содержатся в плодах и овощах, придавая некоторым из них терпкий вкус.
Флаваноны и флаванонолы в свободном виде встречаются редко, чаще в форме гликозидов. Богаты ими цитрусовые плоды, в которых содержатся нарингенин, гесперидин и эридиктол.
Флавоновые пигменты это окрашенные фенольные соединения: антоцианы, флавоны и флавонолы. Эти фенольные гликозиды хорошо растворимы в воде, обладают бактерицидными свойствами. Они содержатся во многих плодах и овощах, отличаются повышенной окислительной способностью. Антоцианы имеют фиолетовый цвет, флавоны и флавонолы желтый.
Антоцианы. Они представляют собой гликозиды, в которых остатки сахаров (глюкозы, галактозы и рамнозы) связаны с окрашенными агликонами, принадлежащими к группе антоцианидинов. Раз- личают шесть антоцианидинов, составляющих агликоны антоцианов пеларгонидин, цианидин, пеонидин, дельфинидин, петунидин, мальвидин. В зависимости от наличия этих соединений плоды имеют разную окраску.
Наиболее распространен цианидин, он обнаружен в яблоках, землянике, сливах и в других плодах. В некоторых плодах антоцианы находятся только в кожице (виноград, слива), в других в кожице и мякоти (малина, черника, смородина).
В зависимости от рН окраска антоцианов может меняться от кра-сной до синей и фиолетовой (в кислой среде красные, в щелочной синие). Антоцианы с ионами К, Nа, Fе и других металлов дают соединения синего цвета.
Флавоны это пигменты, имеющие желтую окраску; содержат-ся во многих плодах и овощах. Флавоны являются предшественниками антоцианов.
Флавонолы отличаются от флавонов наличием гидроксильной группы и обладают сильными бактерицидными свойствами. Чаще всего в плодах и овощах из флавонолов распространены кверцетин, кемферол, рутин и мирицетин. Кверцетин самый распространенный флавонол придает золотистый цвет кожице лука, облепихе.
Полимерные фенольные соединения делятся на гидролизуемые и негидролизуемые конденсированные дубильные вещества.
Гидролизуемые вещества танины это сложные эфиры моносахаридов (глюкозы) и фенольных кислот (галловой, эллаговой, протокатеховой, кофейной, хлорогеновой).
Танины легко подвергаются гидролизу, распадаясь на более простые соединения. Танины взаимодействуют с солями тяжелых металлов, вызывая изменения цвета продуктов переработки плодов и овощей.
Гидролиз дубильных веществ приводит к ослаблению или исчезновению терпкого вкуса плодов и к накоплению сахаров, что улучшает вкус. Кроме того, продукты распада танинов фенольные кислоты усиливают защитные свойства плодов и овощей.
Гидролиз дубильных веществ наблюдается при дозревании плодов и овощей, нанесении механических повреждений и поражении микроорганизмами. Чаще всего при этом накапливается хлорогеновая кислота.
Негидролизуемые вещества состоят из остатков катехинов и лей-коантоцианов и образуются при окислительной конденсации этих мономеров. Конденсация флавоноидов происходит при нагревании с разбавленными кислотами. Конденсированные дубильные вещества с солями железа дают темно-зеленое окрашивание.
Конденсированные дубильные вещества содержат мало углеводов и образуют в присутствии минеральных кислот нерастворимые аморфные соединения флобафены.
Существенным качественным и количественным изменениям подвергаются фенольные соединения в плодах и овощах в процессе созревания и хранения. Количество их уменьшается за счет гидролиза и использования на дыхание. В то же время при созревании плодов и овощей такие фенолы, как антоцианы, флавоны, флаваноны, флавонолы синтезируются и улучшают цвет продуктов. В процессе хранения плодов и овощей происходит взаимопревращение фенольных соединений. Так, при гидролизе танина образуются фенолокислоты, при конденсации катехинов конденсированные дубильные вещества.
Мономерные фенольные соединения.
Фенольные соединения С6 – С1 ряда состоят из ароматического (фенольного) ядра и одноуглеродной боковой цепи.
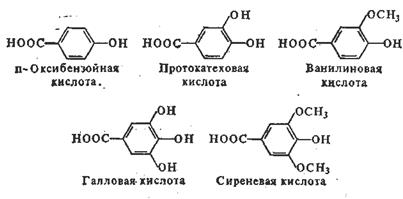 Эта группа соединений представлена в растениях оксибензойными кислотами (оксибензойной, салициловой, протокатеховой, гентизиновой, ванилиновой, галловой, сиреневой), а также соответствующими альдегидами и спиртами.
Эта группа соединений представлена в растениях оксибензойными кислотами (оксибензойной, салициловой, протокатеховой, гентизиновой, ванилиновой, галловой, сиреневой), а также соответствующими альдегидами и спиртами.
Оксибензойные кислоты широко распространены в растениях. Обычно они присутствуют в них в связанном состоянии и освобождаются при гидролизе. Ванилиновая и сиреневая кислоты в виде эфиров входят в состав лигнина, их наличие характерно для древесных растений.
Из С6-С1 – соединений широко известен ванилин (альдегид ванилиновой кислоты), обладающий характерным приятным запахом. В виде глюкозида он содержится в плодах ванили. Ванилин широко применяется в мыловаренной и кондитерской промышленности в качестве душистого вещества. Букет старого коньяка связан с наличием этого вещества. При изготовлении коньяка ванилин образуется в результате окисления кониферилового спирта, содержащегося в клепке дубовых бочек, в которых производится многолетняя выдержка коньяков.
Фенольные соединения С6-С3 ряда состоят из ароматического ядра и трехуглеродной боковой цепи.
К ним относятся производные коричной кислоты – оксикоричные кислоты (n-оксикоричная, кофейная, феруловая, синаповая), а также оксикоричные спирты и кумарины.

Оксикоричные кислоты присутствуют в растениях как в свободном, так и в связанном состоянии. Их особенностью является цис-транс-изомерия.
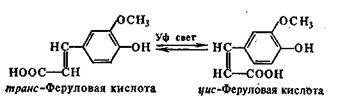
Цис-форма образуется под действием ультрафиолетового облучения, является активатором ростовых процессов.
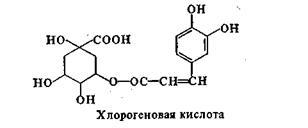 В растениях часто встречаются эфиры оксикоричных кислот с алифатическими и гидроароматическими кислотами. Характерным примером является хлорогеновая кислота. Содержится в прорастающих семенах подсолнечника, необжареных зернах кофе.
В растениях часто встречаются эфиры оксикоричных кислот с алифатическими и гидроароматическими кислотами. Характерным примером является хлорогеновая кислота. Содержится в прорастающих семенах подсолнечника, необжареных зернах кофе.
К подгруппе С6-С3-соединенийотносят оксикоричные спирты. Оксикоричные спирты – исходные компоненты в биосинтезе лигнина.
Кумарин – бесцветная кристаллическое вещество с приятным запахом сена. Кумарины являются производными цис-формы о-оксикоричной (кумариновой 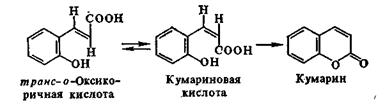 кислоты).
кислоты).
Кумарин и его гидроксилированные производные применяют в табачной и парфюмерной промышленности, в медицине.
Фенольные соединения С6-С3-С6 состоят из двух ароматических ядер (бензольных – А и В), соединенных между собой трехуглеродным фрагментом (гетероциклическим кислородсодержащим кольцом – С).
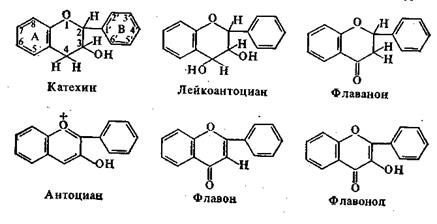
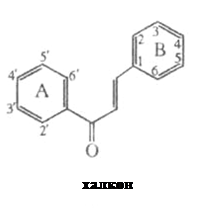 Эта группа соединений особенно разнообразна. Принадлежащие к ней соединения называются также флавоноидами. Флавоноиды являются наиболее распространенной группой фенольных соединений и в зависимости от степени окисленности их трехуглеродного фрагмента делится на 10 основных подгрупп: катехины, лейкоантоцианиды (лейкоантоциан), флаваноны, флаванонолы, дигидрохалконы, халконы, ауроны, флавоны, антоцианидины (атоциан), флавонолы.
Эта группа соединений особенно разнообразна. Принадлежащие к ней соединения называются также флавоноидами. Флавоноиды являются наиболее распространенной группой фенольных соединений и в зависимости от степени окисленности их трехуглеродного фрагмента делится на 10 основных подгрупп: катехины, лейкоантоцианиды (лейкоантоциан), флаваноны, флаванонолы, дигидрохалконы, халконы, ауроны, флавоны, антоцианидины (атоциан), флавонолы.
Фенольные соединения – Антоцианы винограда
Содержание материала
Это красящие вещества ягод, плодов и цветочных лепестков, а также листьев некоторых растений. Первые исследования по изучению химического строения антоцианов были проведены Р. Вилыптеттером, П. Каррером и В. Робинсоном.
Антоцианы широко распространены в растительном мире. Основными представителями их являются следующие агликоны: цианидол, дельфинидол, петунидол, мальвинидол и пеларгонидол. Ниже приведена структурная формула дельфинидола.
В винограде, в зависимости от его рода и вида, было найдено от семи до семнадцати веществ, являющихся моно- и дигликозидами, а также — ряд веществ в виде ацилированных гетерозидов, которые соединены с ароматическими кислотами, такими как, например, n-оксибензойная, n-оксикоричная, n-кумаровая.
В гликозидах антоцианидинов остаток сахара присоединяется в случаях моногликозидов к углеродному атому в положении 3, а в случае дигликозидов — в положении 5. Из сахаров, входящих в молекулу антоцианов, главным образом встречается глюкоза, реже рамноза, арабиноза и галактоза.
Красящие вещества ягод винограда находятся как в свободном состоянии — это, так называемые антоцианидины, так и в связанном с сахарами в виде гликозидов — это антоцианы. Антоцианы содержат в гетероциклическом кольце четырехвалентный кислород (оксоний) и благодаря этому легко образуют соли, например хлориды.
Цвет антоцианов зависит от природы металла, который входит в их комплекс. С железом антоцианы дают синюю, с молибденом фиолетовую, с никелем белую, с кальцием пурпурную окраску. Цвет антоцианов также зависит от pH среды, в зависимости от которого появляется окраска, образуемая псевдооснованиями. Так, например, при подкислении антоцианы окрашиваются в красный цвет, а при подщелачивании приобретают голубоватый, а в сильно щелочной среде зеленоватый цвет. Это явление имеет важное значение в виноделии. Образование псевдооснования обусловливает интенсивность окраски красных вин в зависимости от их pH.
Антоцианы в основном распределены в кожице винограда. Они, находятся в третьем или четвертом слое гиподермы, а в мякоти под гиподермой. Внутри клеток антоцианы концентрируются в вакуолях в виде гранул. Цитоплазма и стенки клеток их не содержат. Но когда клетка погибает, то в результате диффузии окрашивается вся ткань [105].
Известно, что при сульфитации красных вин интенсивность их окраски уменьшается. Объясняется это тем, что антоцианы способны образовывать псевдооснования. Это явление обратимо. Так, если к обесцвеченному вину добавить уксусный альдегид, то оно вновь приобретает окраску. Известно, что сернистая кислота связывается с уксусным альдегидом и образует альдегидсернистую кислоту.
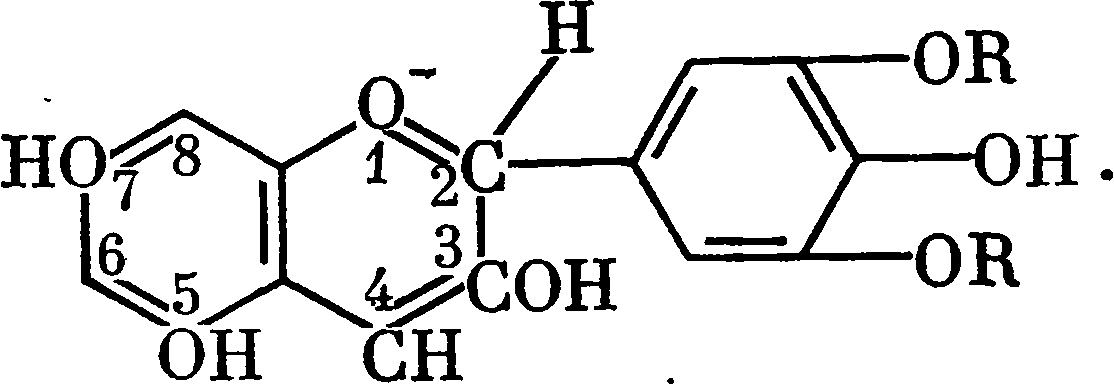
П. Риберо-Гайон [155] показал, что под влиянием сернистой кислоты в антоцианах происходят следующие структурные молекулярные изменения:

При действии SO2 трехуглеродистый фрагмент С размыкается и SO2 присоединяется ко второму и третьему углероду, образует дисульфосоединение, в результате чего и происходит обесцвечивание среды.
Дигликозиды проявляют большую стойкость к обесцвечиванию, чем моногликозиды, но дигликозиды склонны к покоричневению, вызываемому окислением. Мальвидол, пеонидол более устойчивы, а дельфинидол менее устойчив к окислению. Присутствие танина защищает антоцианы от разрушения под действием ультрафиолетовых лучей, n-бензохинон способствует обесцвечиванию антоцианов.
В последнее время из белого винограда сорта Мюллер-Тургау методом жидкостной хроматографии было выделено до 300 мг/л процианидинов. На сефадексе LH-20 были разделены фракции процианидинов, состоящие из смеси двух стереоизомерных форм, — тримеров (триэпикатехин и катехин-эпикатехин), галлокатехина и катехингаллата [129].
Биосинтез антоцианов. Биосинтез антоцианов в растениях сходен с биосинтезом флавонолов, при этом флороглюциновое кольцо образуется из ацетил-КоА, т. е. из активированного ацетата, а пирокатехиновое и пирогаллоловое кольца — через шикимовую кислоту.
Биосинтетический путь антоцианов и флавонолов протекает вначале одинаково. С помощью меченого С14 фенилаланина показано, что это соединение включается как в антоцианы, так в лейкоантоцианы и флавонолы. В отличие от других флавоноидов образование антоцианов происходит на свету. Но существует и другое мнение, что антоцианы синтезируются только в темноте, а при действии света происходит их распад. По мнению других исследователей, в темноте образуются лейкоантоцианы, которые при освещении переходят в антоцианы. Согласно данным С. В. Дурмишидзе [29], антоцианы синтезируются как на свету, так и в темноте, но на свету их образуется в 2 раза больше. Интенсивность освещения листьев винограда влияет на скорость образования антоцианов.
Биологическая роль антоцианов еще мало изучена. Одни считают, что они служат защитой от ультрафиолетового излучения, другие связывают появление антоцианов с заболеванием растений, третьи полагают, что они обусловливают иммунитет растений. Было высказано предположение, что антоцианы играют определенную роль в холодостойкости растений.
Антоцианы винограда и вина. По данным П. Риберо-Гайона (1964), в зависимости от вида и рода виноградной лозы было найдено от шести до семнадцати антоцианов, являющихся моногликозидами, дигликозидами и гетерозидами. Согласно его исследованиям дигликозиды антоцианов никогда не встречаются в ягодах европейских сортов винограда вида Vitis vinifera, содержатся только в гибридах вида Vitis riparia и Vitis rupestris. Исследуя европейские сорта, культивируемые во Франции, он не смог обнаружить в них антоциановые дигликозиды.
Основываясь на этом, П. Риберо-Гайон хроматографическим методом исследовал вина, приготовленные из винограда европейских сортов (как не содержащие дигликозидов), и вина, приготовленные из гибридного винограда (как содержащие дигликозиды).
Некоторые исследователи подтвердили данные П. Риберо-Гайона и также установили, что в европейских сортах винограда, произрастающих не только во Франции, но и в других странах, не содержатся дигликозиды.
С. В. Дурмишидзе, А. Н. Сапромадзе (1960) показали, что в винограде некоторых европейских сортов (Алеатико, Морастель, Португизер, Оберлен и др.), произрастающих в Грузии, содержатся дигликозиды антоцианов. С. В. Дурмишидзе и его сотрудники методом хроматографии на бумаге изучили состав антоцианов винограда около 100 сортов, культивируемых в Грузии в разных экологических условиях. Эти исследования показали, что в кожице винограда в большинстве случаев содержатся моногликозиды дельфинидола, петунитола, пеониодола и мальвинидола, который преобладает. В некоторых сортах также были найдены дигликозиды петунидола и мальвинидола. Так, в сорте Асуретули Шави содержится до 17% дигликозидов петунидола и мальвинидола, в сортах Саперави и Каберне Совиньон урожая 1961 г.— 6,6%, а винограде 1962 г. отсутствуют. Наименьшее количество этих дигликозидов было найдено в винограде сорта Алеатико — всего 2%.
С. В. Дурмишидзе с сотрудниками (1960) исследовал также состав антоцианов в кожице винограда. На основании полученных данных он пришел к заключению, что между европейскими сортами винограда и гибридами, произрастающими в Грузии, нет резкого различия в содержании антоцианов.
Л. Дибнер и М. Бурцо установили, что дигликозиды в гибридных сортах винограда локализированы в кожице, вследствие чего при переработке винограда по белому способу в винах невозможно обнаружить дигликозиды.
Установлено, что динамика накопления фенольных соединений, в частности антоцианов, в период созревания винограда происходит медленно, а при перезревании наблюдается уменьшение их количества. Накопление антоцианов по мере созревания винограда протекает параллельно с накоплением сахаров и продолжается в течение двух недель, а затем начинает уменьшаться.
По данным П. Риберо-Гайона [156], в период формирования ягод и в начале созревания винограда первым появляется цианидол, затем происходит его метоксилирование с образованием пеонидола. Из цианидола образуется дельфинидол, а из него путем метоксилирования получается петунидол и мальвинидол.
В количественном отношении антоцианы в ягодах красных сортов винограда распределяются следующим образом: мальвинидол- 3-моноглюкозид 49,8%, пеонидол-3-моноглюкозид 36,9%, циани- дол-3-моноглюкозид 8,75%, петунидол-3-моноглюкозид 4,05%. Найдены также коффенилмальвидол-3-гликозид, n-кумароил-мальви- дол-3-глюкозид. Недавно был найден в красных сортах винограда моногликозид пеларгодин [158]. Некоторые авторы считают, что в винограде содержится система энзимов, которая способна разлагать антоцианы. При этом разложение осуществляется только в присутствии пирокатехина. Исходя из этого, Р. Каррено и Р. Диаз (1969) предположили, что речь идет о связанной системе энзимов. Оптимальное значение pH при разложении антоцианов винограда сорта Каберне Совиньон лежит при 5,2—5,4. Как показали исследования В. Сегаля (1969), энзиматическому окислению способствует полифенолоксидаза, которая в присутствии пирокатехина энергично расщепляет антоцианы.
По нашему мнению о-дифенолоксидаза окисляет пирокатехин с образованием о-хинонов, которые усиливают окислительные процессы, приводящие к разрушению антоцианов.
Г. Г. Валуйко и А. И. Иванютина (1967) изучали ингибирующее действие антоцианов (как гликозидов, так и агликонов) на жизнедеятельность винных дрожжей и установили, что наиболее активным действием обладает пеонидин как моноглюкозид, так и его агликон. Мальвинидин, петунидин и дельфинидин, по данным этих авторов, менее активны.
Источники:
http://studwood.ru/1725840/matematika_himiya_fizika/fenolnye_soedineniya
http://helpiks.org/5-107748.html
http://vinograd.info/knigi/osnovy-biohimii-vinodeliya/fenolnye-soedineniya-4.html




